Clínica Cotidiana
Información del artículo
Historia del artículo:
Recibido el 16 de noviembre de 2015
Aceptado el 24 de octubre de 2016
On-line el 20 de febrero de 2017
Palabras clave:
Adenocarcinoma
Vesícula
Biliar
Litiásica
Carcinosis
Peritoneal
*Autor para correspondencia
Correo electrónico:
hermidana@yahoo.es
(J.A.Hermida Pérez).
Keywords:
Adenocarcinoma
Bladder
Bile
Gallstone
Carcinosis
Peritoneal
José Alberto Hermida Pérez
Centro Salud El Paso. Santa Cruz de Tenerife.
Resumen
El cáncer de la vesícula biliar es la neoplasia maligna más frecuente del tracto biliar.
Pese a los recientes avances en las técnicas de diagnóstico por imagen, se detecta usualmente en estadios avanzados debido a la falta de síntomas y signos específicos de presentación, por lo que se ha asociado clásicamente a un pésimo pronóstico. La supervivencia global a 5 años en las series más numerosas está por debajo del 5 % y la mediana de supervivencia es de menos de 6 meses. No obstante, el papel de la cirugía radical se está definiendo de forma más clara recientemente.
Es esencial para el Médico de Familia conocer la alta posibilidad que existe de que estas lesiones sean diagnosticadas en estadios avanzados, así como los factores de riesgo, epidemiológicos y características clínicas asociados al desarrollo de las mismas.
@ 2017 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Gallbladder adenocarcinoma, gallstone and peritoneal carcinomatosis in a young woman
Abstract
Gallbladder cancer is the most common malignancy of the biliary tract.
In spite of the recent advances in imaging techniques is usually detected in advanced stages due to lack of specific symptoms and signs of submission, which has been classically associated with a dismal prognosis. Overall survival at 5 years in the largest series is below 5%, and median survival is less than 6 months. However, the role of radical surgery is being defined more clearly recently.
It is essential for family doctors know that there is high possibility that these lesions are diagnosed in advanced stages, and the risk factors associated with epidemiological and development of the same clinical characteristics.
@ 2017 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A
Mujer de 49 años de edad, con antecedentes personales de dolor abdominal crónico recurrente, difuso, más intenso en el hipocondrio derecho y el epigastrio, pérdida de 3 kilos de peso, anemia ferropénica, gastroduodenitis y extirpación de un pólipo hiperplásico benigno en el colon sigmoide. Antecedentes familiares: padre fallecido de carcinoma de colon.
Como protocolo de estudio del dolor abdominal se realiza analítica: aspartato-aminotransferasa 217 UI/L, alanino-aminotransferasa 374 UI/L, gamma-glutamiltransferasa 67,7 UI/L, eritrosedimentación 113 mm, fosfatasa alcalina 109 UI/L, antígeno carcinoembrionario 8,17 ng/ml, antígeno Ca 19,9 82,20 UI/ml, hematíes 4,42 106/µl, hemoglobina 12,3 g/dl, hematocrito 35,5 %, volumen corpuscular medio 80,3 mm3.
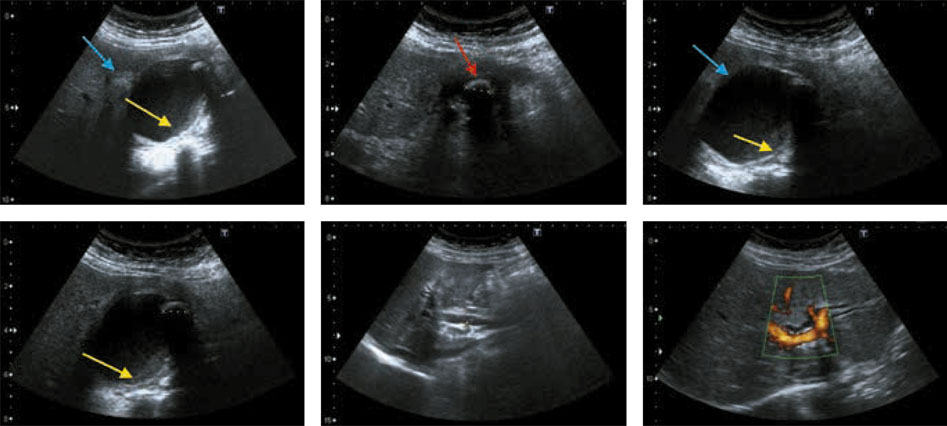
Ecografía abdominopélvica (Fig. 1): moderada cantidad de líquido libre intraperitoneal, vesícula biliar (VB) con pared de aspecto patológico, sobre todo en la región del fundus, engrosada; en el fundus hay un cálculo de unos 13 mm; en parte de la luz vesicular hay material ecogénico, posiblemente litiásico. Parénquima hepático: inmediatamente por encima de la vesícula se observan zonas pseudonodulares de mayor ecogenicidad. Los hallazgos sugieren proceso inflamatorio vesicular bastante evolucionado. Conducto hepático común, derecho e izquierdo ligeramente dilatados; el colédoco alcanza un calibre de unos 8,6 mm, sin identificar lesiones obstructivas. Páncreas, riñones y bazo, sin evidencia de patología. Útero aumentado de tamaño, de aspecto miomatoso. Imagen quística anexial derecha.
Se remite a Cirugía General, donde se decide realizar colecistectomía laparoscópica. En el acto quirúrgico se detectan múltiples implantes peritoneales sugestivos de carcinocis peritoneal y proceso inflamatorio perivesicular. Se toman muestras para anatomía patológica (AP) cuyo informe es: metástasis peritoneales de adenocarcinoma de VB (ADC VB). No se realiza la colecistectomía.
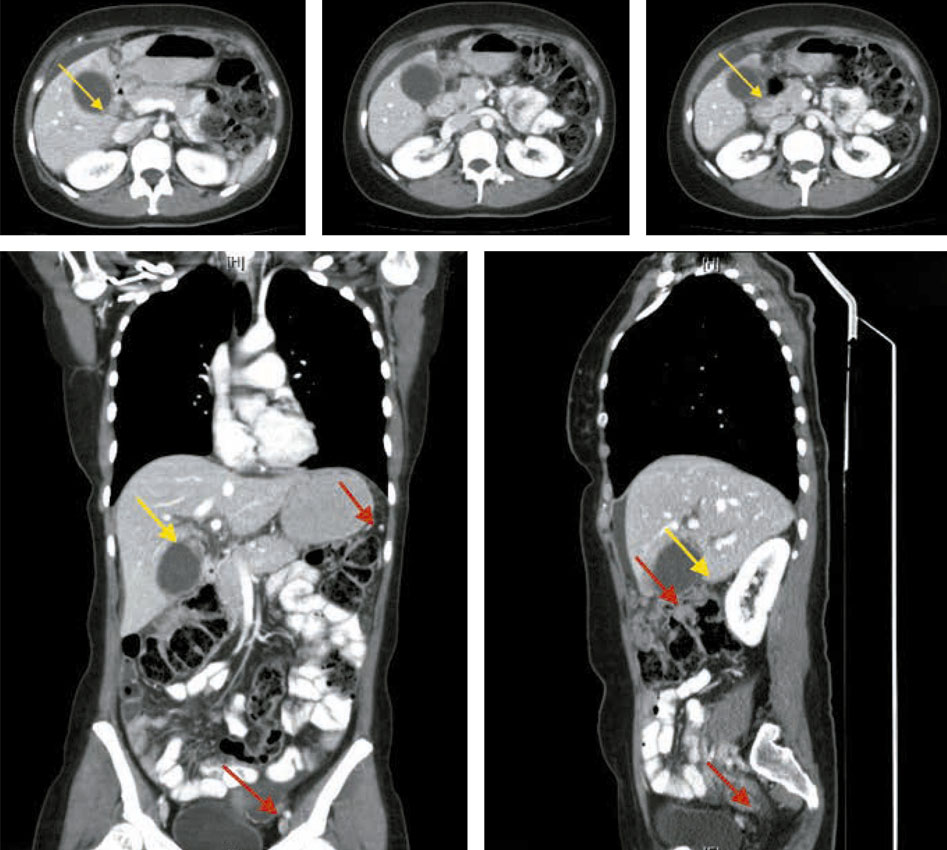
Se indica TAC de abdomen superior y pelvis sin y con contraste (Fig. 2): vías intrahepáticas y hepático común dilatados, colédoco con calibre de 8 mm; vesícula distendida con litiasis y barro en su interior, con paredes engrosadas; alteración en la densidad del parénquima hepático circundante; alteración de la densidad de la grasa subhepática; múltiples nódulos que afectan a la grasa omental compatible, con una carcinomatosis peritoneal con líquido libre asociado. Dichos hallazgos sugieren la existencia de un proceso neoformativo. Útero globuloso con líquido en la cavidad endometrial.
La paciente es remitida a Oncología. Actualmente se encuentra en tratamiento quimioterapéutico.
Figura 1 – Ecografía abdominopélvica: moderada cantidad de líquido libre intraperitoneal; vesícula biliar con pared de aspecto patológico, sobre todo en la región del fundus, engrosada (flechas amarillas); en la región fúndica hay un cálculo de unos 13 mm (flecha roja); en el parénquima hepático, inmediatamente por encima de la vesícula, se observan zonas pseudonodulares de mayor ecogenicidad (flecha azul); conductos hepáticos comunes, derecho e izquierdo ligeramente dilatados, colédoco con calibre de unos 8,6 mm, sin identificar lesiones obstructivas; páncreas, riñones y bazo, sin evidencia de patología.
Figura 2 – TAC de abdomen superior y pelvis sin y con contraste: vías intrahepáticas y hepático común dilatado; el colédoco tiene un calibre de 8 mm; vesícula distendida con litiasis y barro en su interior, paredes engrosadas y alteración en la densidad del parénquima hepático circundante (flecha amarillas); existe una alteración de la densidad de la grasa subhepática así como múltiples nódulos que afectan a la grasa omental compatible con una carinomatosis peritoneal (flechas rojas).
Comentario
El carcinoma de VB (CVB) fue descrito por primera vez por Maximillian de Stoll en 17771. Sin embargo, la primera resección por esta patología se atribuye a Keen en 1891, y fue posteriormente George Pack, en 1955, el primer cirujano que realizó una resección hepática radical para el tratamiento de un CVB2.
El cáncer de VB (CVB) representa 2-4 % de las afecciones malignas gastrointestinales. Se encuentra en forma casual en la evaluación AP de 0,3-5 % de todas las piezas de colecistectomía. Es la quinta neoplasia más común del tubo digestivo. De ellos, 80 % son adenocarcinomas (ADC) y el resto son tumores indiferenciados o de células escamosas. Se reportan incidencias de 2-7 % para el cáncer indiferenciado, 1-6 % para el carcinoma de células escamosas, y 1-4 % para el adenoescamoso.
El sexo femenino, edad mayor de 50 años y la presencia de litiasis acompañan la mayoría de los casos de CVB. Al parecer, la litiasis desencadena una respuesta inflamatoria con liberación de factores de crecimiento (promotores tumorales) y estos ejercen su efecto sobre un epitelio dañado previamente por otros agentes3,4.
El CVB se presenta con mayor frecuencia en la mujer, con una relación de 1,7:1. Son factores predisponentes la colelitiasis (70-90 % de casos), tumores benignos, anormalidades de la unión de los conductos pancreatobiliares y edad avanzada, entre otros. La colesterolosis fue el hallazgo más común en las piezas de colecistectomía: de cada 1.000 colecistectomías realizadas en 5,4 existía algún tipo de CVB (0,54 %). El ADCVB es el más común: 88 % del total de los CVB3,6.
El 99 % de los CVB se originan en el epitelio, y de ellos el 95 % son ADC. Algunos factores de riesgo (FR) estrechamente vinculados con el CVB son7-9:
- Colelitiasis. No se ha podido demostrar una relación causa-efecto absoluta. Es el principal FR vinculado con el CVB. La litiasis vesicular puede ser un factor etiológico, ya que acompaña a las neoplasias en 80-90 % de los casos. Otros factores relacionados con la patogenia de los cálculos y que ejercen influencia indirecta son sexo femenino, embarazo, ingestión de estrógenos exógenos, obesidad, historia familiar de colelitiasis, toma de ciertos fármacos (clofibrato), afecciones digestivas (enteritis regional segmentaria, fibrosis quística), procedimientos quirúrgicos (vagotomías tronculares, resecciones gástricas) y otras varias enfermedades (síndromes hemolíticos o de inmunodeficiencia).
- Vesícula en porcelana. Se asocia con CVB en 12-61 % según las distintas series (promedio de 25 %), aunque no está del todo demostrado.
- Infección de la VB. La estasis biliar, la inflamación crónica y la infección pueden inducir transformación carcinomatosa del epitelio vesicular. Los portadores crónicos de Salmonella typhi y paratyphi tienen mayor riesgo de desarrollar neoplasia; otros microorganismos, como Clostridium aislado en la bilis parecen ser responsables de la producción de sustancias carcinogenéticas.
- Tumores benignos de VB. Los pólipos de colesterol no son susceptibles de transformación neoplásica; los adenomas y papilomas sí pueden degenerar.
- Anomalías de la vía biliar. Especialmente de la desembocadura del Wirsung, en particular la configuración del tipo “conducto común” (incidencia de 16,7 % en el CVB). Parece haber una inflamación crónica de la vesícula biliar debida al reflujo continuo y no controlado de jugo pancreático.
- Agentes carcinógenos: ácido litocólico, metilcolantreno, aminoazatolueno, nitrosaminas, caucho, fármacos: metildopa, los anticonceptivos orales y la isoniazida (no demostrado con certeza).
- Otras: colitis ulcerosa, determinadas formas de parasitosis y el humo del tabaco.
En general, los síntomas tempranos están ausentes y son inespecíficos. Muchos de los casos se diagnostican histológicamente después de una colecistectomía. Los tumores avanzados pueden manifestarse con ictericia, por compresión de la vía biliar.
Otras manifestaciones: dolor abdominal, mal vaciamiento gástrico por compresión del duodeno, fiebre y prurito.
En ocasiones se detecta una masa abdominal palpable o por adenopatías supraclaviculares.
La ecografía puede mostrar masas intraluminales que hagan suponer la presencia de una neoplasia; sin embargo, en nuestro medio esto es infrecuente y en general se asocia a tumores avanzados y de mal pronóstico. Ocasionalmente el diagnóstico ecográfico preoperatorio se logra en pacientes con neoplasias papilares con crecimiento hacia la luz vesicular.
La TAC y la RMN permiten definir el nivel de obstrucción y el compromiso de estructuras vecinas y de vasos sanguíneos.
La colangiografía endoscópica retrógrada y la colangiografía transparietohepática son útiles. En ocasiones se requiere de una laparoscopia diagnóstica con o sin ultrasonografía intraoperatoria o de una laparotomía para certificar el diagnóstico y la posibilidad de resección3-5.
En general la posibilidad de resección de los pacientes con CVB es baja (15-20 %) debido al diagnóstico tardío. Esto empeora notablemente el pronóstico general, con sobrevidas que no superan el 5 % a los 5 años.
En pacientes sintomáticos y con pólipos, se aconseja la colecistectomía; en los asintomáticos con pólipos de hasta 5 mm, observación y seguimiento ecográfico (más del 90 % constituidos por cristales de colesterol). En caso de pólipos de 10 mm o más, y que experimentan crecimiento, se aconseja la colecistectomía debido al aumento en frecuencia de lesiones neoplásicas con potencial maligno.
La cirugía radical puede ser curativa en pacientes con tumores confinados a la pared de la vesícula, con compromiso mucoso o de la muscular, con compromiso del tejido conectivo perimuscular y sin compromiso de la serosa. En estos pacientes la supervivencia a 5 años puede ascender a 30-85 %. En los tumores más superficiales la simple colecistectomía se considera terapéutica y potencialmente curativa.
La quimio y la radioterapia neoadyuvante y adyuvante se encuentran en etapa de evaluación y por ahora deben ser empleadas en protocolos controlados.
En los pacientes diagnosticados en estadios más avanzados (metástasis) la intervención quirúrgica está contraindicada. Se puede valorar la quimioterapia y otros tratamientos con cuidados paliativos. El prurito y la ictericia pueden tratarse mediante drenaje de la vía biliar. La obstrucción duodenal puede requerir en ocasiones de una laparotomía más gastroenteroanastomosis para permitir la alimentación oral, siempre y cuando las condiciones del paciente y esperanza de vida lo permitan3-5,10.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- De Stoll M. Rationis mendendei in nosocomia. En: Practico Unindobonensi, parte I. Viena: Berardi; 1777. p. 290.
- Pack GT, Miller TR, Brasfiled RD. Total right hepatic lobectomy for cancer of the gallbladder. Ann Surg. 1955; 142: 6-16.
- De la Parra-Márquez ML, Martínez-Garza H, Sánchez-Antúnez D, Cabañas-López A, Ramírez-Garza M, González-Quintanilla A. Adenocarcinoma de vesícula biliar como hallazgo histopatológico posterior a colecistectomía. Cir Ciruj. 2005; 73: 97-100.
- Cortés A, Botero MP, Carrascal E, Bustamante F. Carcinoma insospechado de vesícula biliar. Colomb Med. 2004; 35: 18-21.
- Ramírez CP, Suárez MA, Santoyo J, Fernández JL, Jiménez M, Pérez JA, et al. Actualización del diagnóstico y el tratamiento del cáncer de vesícula biliar. Cir Esp. 2002; 71: 102-11.
- Castillo García JJ, Romo Aguirre C, Ruiz Lizárraga J, Escrivá Machado JF, Córdova Pluma II VH. Cáncer de vesícula biliar como hallazgo histopatológico posterior a la colecistectomía. Prevalencia e incidencia en el Hospital Ángeles Pedregal. Acta Med Grupo Ángeles. 2010; 8: 140-7.
- Ríos P, Aguilar L, Ríos P. Cáncer de vesícula biliar-estrategia quirúrgica: a propósito de un caso incidental re-resecado en el hospital Rebagliati. Rev Gastroenterol Perú. 2009;29:374-7.
- Morera F, Ballestín J, Ripoll F, Landete F, García-Granero M, Millán J, et al. Cáncer de vesícula biliar en un hospital comarcal. Cir Esp. 2009; 86: 219-23.
- Seguel G, Fres E, Frez M, Pinochet F, Espinosa R, Suárez J. Naturaleza de los pólipos de la vesícula biliar sometidos a colecistectomía. Rev Chil Cir. 2007; 59: 208-11.
- Ramos-Font C, Santiago A, Rodríguez-Fernández A, Rebollo A, Gómez M, Llamas J. Estatificación del cáncer de vesícula mediante tomografía de positrones con 18F-fluorodesoxiglucosa. Rev Esp Med Nucl. 2009; 28: 74-7.