Documento de consenso
Información del artículo
Historia del artículo:
Recibido el 12 de julio de 2016
Aceptado el 12 de julio de 2016
On-line el 20 de febrero de 2017
Palabras clave:
Síndrome del intestino irritable
Estreñimiento funcional
Molestia abdominal
Adultos. Atención Primaria
Enfermedades Digestivas
Guía de Práctica Clínica
Roma IV
*Autor para correspondencia
Correo electrónico:
pcanonesg@semg.es
(Pedro Cañones)).
http://dx.doi.org/10.24038/mgyf.2017.005
*Este trabajo se publica conjuntamente por la SEPD, la semFYC, la SEMERGEN y la SEMG. La publicación original íntegra se realizó por la SEPD en Rev Esp Enferm Dig 2016; 108: 332-3631. semFYC73, SEMERGEN74 y SEMG publican el trabajo en dos partes, para accesibilidad de sus respectivos socios; esta es la primera.
Nota Metodológica: Esta GPC ha sido desarrollada entre enero de 2015 y diciembre de 2015 por un Grupo de Trabajo formado por expertos seleccionados por la SEPD, la semFYC, la SEMERGEN y la SEMG. Entre diciembre de 2015 y abril de 2016 fue sometida a revisión, con la última adaptación a Roma IV en mayo de 20161.
Para un detalle del proceso metodológico de trabajo mediante el cual se ha elaborado esta GPC ver http://www.sepd.es/file/GPC_SII_E_EF_Metodologia.pdf
Fermín Mearina,*, Constanza Cirizab, Miguel Mínguezc, Enrique Reyd, Juan José Mascorte, Enrique Peñaf, Pedro Cañonesg, Javier Júdezh, para la SEPD, la semFYC, la SEMERGEN y
la SEMG
Sociedad Española de Patología Digestiva (SEPD), Sociedad Española de Medicina de Familia y Comunitaria (semFYC), Sociedad Española de Médicos de Atención Primaria (SEMERGEN), Sociedad Española de Médicos Generales y de Familia (SEMG)
aCoordinador de la GPC. Comité Roma de Trastornos Funcionales Intestinales. Miembro AEG. Centro Médico Teknon. Barcelona. bGrupo de Trastornos Funcionales. SEPD. Hospital Universitario Doce de Octubre. Madrid. cMiembro AEG y SEPD. Hospital Clínico Universitario. Universitat de Valencia. Valencia. dSEPD. Hospital Clínico Universitario San Carlos. Madrid. eSecretario Científico. semFYC. fCoordinador de Digestivo. SEMERGEN. gCoordinador de Digestivo. SEMG. hDepartamento de Gestión del Conocimiento. SEPD.
Resumen
En esta Guía de Práctica Clínica analizamos el manejo diagnóstico y terapéutico de pacientes adultos con estreñimiento y molestias abdominales, bajo la confluencia del espectro del síndrome del intestino irritable y el estreñimiento funcional. Ambas patologías están encuadradas en los trastornos funcionales intestinales y tienen una importante repercusión personal, sanitaria y social, afectando a la calidad de vida de los pacientes que las padecen. La primera es el subtipo de síndrome del intestino irritable en el que el estreñimiento es la alteración deposicional predominante junto con dolor abdominal recurrente, hinchazón y distensión abdominal frecuente. El estreñimiento se caracteriza por la dificultad o la escasa frecuencia en relación con las deposiciones, a menudo acompañado por esfuerzo excesivo durante la defecación o sensación de evacuación incompleta. En la mayoría de los casos no tiene una causa orgánica subyacente, siendo considerado un trastorno funcional intestinal. Son muchas las similitudes clínicas y fisiopatológicas entre ambos trastornos, con respuesta similar del estreñimiento a fármacos comunes, siendo la diferencia fundamental la presencia o ausencia de dolor, pero no de un modo evaluable como “todo o nada”. La gravedad de estos trastornos depende no sólo de la intensidad de los síntomas intestinales sino también de otros factores biopsicosociales: asociación de síntomas gastrointestinales y extraintestinales, grado de afectación, y formas de percepción y comportamiento. Mediante los criterios de Roma, se diagnostican los trastornos funcionales intestinales. Esta Guía de Práctica Clínica está adaptada a los criterios de Roma IV difundidos a finales de mayo de 2016 y analiza, en esta primera parte, los aspectos conceptuales y fisiopatológicos, los criterios de alarma, las pruebas diagnósticas y los criterios de derivación entre Atención Primaria y Aparato Digestivo. En una segunda parte, se revisarán todas las alternativas terapéuticas disponibles (ejercicio, ingesta de líquidos, dieta con alimentos ricos en fibra soluble, suplementos de fibra, otros componentes de la dieta, laxantes osmóticos o estimulantes, probióticos, antibióticos, espasmolíticos, esencia de menta, prucaloprida, linaclotida, lubiprostona, biofeedback, antidepresivos, tratamiento psicológico, acupuntura, enemas, neuroestimulación de raíces sacras o cirugía), efectuando recomendaciones prácticas para cada una de ellas.
© 2017 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Clinical Practice Guide. Irritable bowel syndrome with constipation and functional constipation in adults. Concept, diagnosis and care continuity (Part 1)
Keywords:
Irritable bowel syndrome
Functional constipation
Abdominal discomfort
Adults. Primary Care
Digestive diseases
Clinical Practice Guide
Rome IV
Abstract
In this Clinical Practice Guide, we analyze diagnostic and therapeutic management of adult patients with constipation and abdominal discomfort, under the confluence of the spectrum of the irritable bowel syndrome and functional constipation. Both conditions are located within intestinal functional disorders and have a significant personal, health and social repercussion, affecting quality of life of the patients who suffer them. The former is the subtype of irritable bowel syndrome in which constipation is the predominant bowel movement alteration together with recurrent abdominal pain, swelling and frequent abdominal distension. The constipation is characterized by difficulty or scarce frequency in relation with bowel movements, often accompanied by excessive effort during defecation or sensation of incomplete evaluation. There is no underlying organic cause in most of the cases, it being considered a functional intestinal disorder. There are many clinical and physiopathological clinical similarities between both disorders, with similar response of the constipation to common drugs, the fundamental difference being the presence or absence of pain, but not in an “all or nothing” evaluable way. The severity of these disorders depends not only on the intensity of the intestinal symptoms but also on other biopsychosocial factors: association of gastrointestinal and extraintestinal symptoms, grade of impairment, forms of perception and behavior. Using the Rome criteria, the functional gastrointestinal disorders are diagnosed. The Clinical Practice Guide is adapted to the Rome IV criteria dissiminated at the end of May 2016 and analyzes, in this first part, the conceptual and pathophysio aspects, alarm criteria, diagnostic tests and referral criteria between Primary Care and Digestive Tract Department. In a second part, all the available therapeutic alternatives will be reviewed (exercise, fluid intake, diet with soluble fiber rich foods, fiber supplements, other components of the diet, osmotic or stimulants laxatives, probiotics, antibiotics, spasmolytics, peppermint essence, prucalopride, linaclotide, lubiprostone, biofeedback, antidepressants, psychotherapy, acupuncture, enemas, sacral nerve stimulation or surgery), with practical recommendations for each one of them.
© 2017 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A
Aspectos conceptuales, impacto y fisiopatología
1. ¿Por qué abordar el síndrome del intestino irritable con estreñimiento y el estreñimiento funcional en el adulto conjuntamente?
El síndrome del intestino irritable (SII) y el estreñimiento funcional (EF) son dos trastornos funcionales intestinales (TFI)2,3. Por tanto, ambos comparten que su causa no se explica por las alteraciones morfológicas, metabólicas o neurológicas demostrables por las técnicas diagnósticas habituales. El SII se divide, de acuerdo al tipo de alteración del hábito deposicional predominante, en SII con estreñimiento (SII-E) y SII con diarrea (SII-D); cuando se combinan ambos trastornos, estreñimiento y diarrea, se habla de SII de tipo mixto (SII-M) y SII de tipo indeterminado (SII-I) cuando el patrón de las deposiciones es intermedio y no puede clasificarse como diarrea ni estreñimiento2,3.
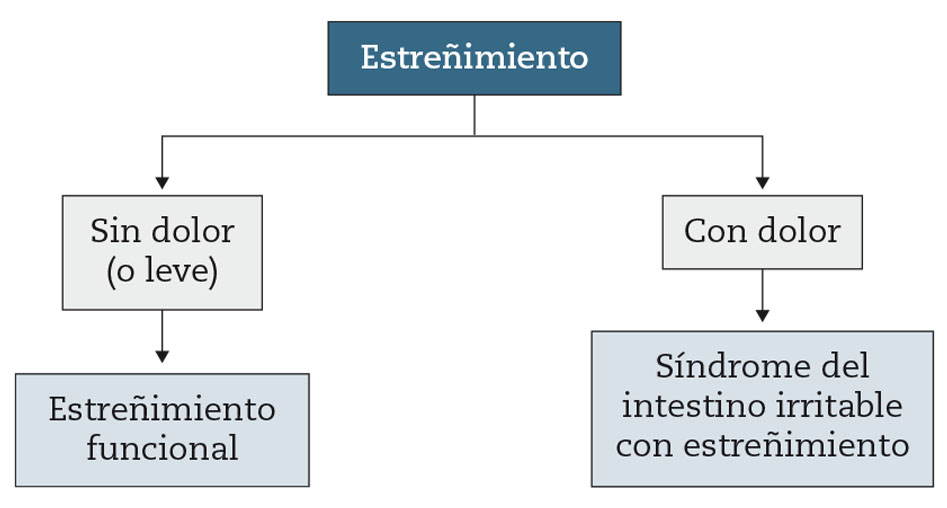
Aunque desde un punto de vista conceptual el SII-E y el EF son dos TFI diferentes, en la práctica pueden ser muy parecidos e incluso indistinguibles4-6. En los dos el estreñimiento es un síntoma primordial, como también lo es la hinchazón/distensión del abdomen. La presencia de dolor abdominal más de una vez a la semana, y la relación temporal del dolor con la defecación, es lo que teóricamente diferencia al SII-E del EF2. Sin embargo, puede haber pacientes con EF y un cierto grado de dolor y la relación temporal no siempre es fácil de establecer4. En realidad, el SII-E y el EF forman un espectro en el que en un extremo estarían los pacientes con dolor abdominal muy importante junto con estreñimiento, y en el otro los pacientes con estreñimiento y ausencia absoluta de dolor; en la práctica, la mayoría de casos están en un lugar intermedio. De hecho, pudiera ser más lógico clasificar este tipo de TFI de la siguiente manera: estreñimiento con dolor (similar al SII-E) y estreñimiento sin dolor (similar al EF) (Fig. 1).
Además de estas similitudes conceptuales y clínicas, el SII-E y el EF tienen diversos mecanismos patogénicos comunes y en ambos se han demostrado respuestas beneficiosas a los mismos fármacos7-12.
Todos los aspectos anteriores nos han movido a realizar una GPC en la que se abordan de manera conjunta el SII-E y el EF. Sin duda, entre ellos hay más semejanzas que diferencias.
2. ¿Qué es el síndrome del intestino irritable?
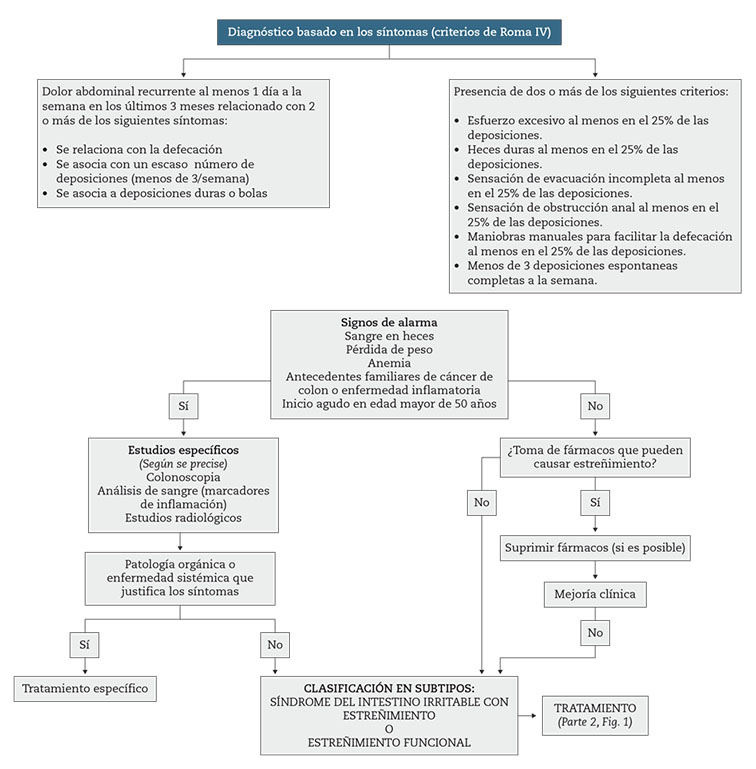
El SII se caracteriza por la presencia de dolor abdominal recurrente asociado a alteraciones del ritmo deposicional, ya sea en forma de estreñimiento, de diarrea, o de ambas; la hinchazón y la distensión abdominal son muy frecuentes en el SII2,3. De acuerdo a los criterios de Roma IV el SII se diagnostica por la presencia de dolor abdominal recurrente que debe estar presente al menos un día a la semana, con dos o más de las siguientes características: 1. Se asocia a la defecación; 2. Está relacionado con un cambio en la frecuencia de las deposiciones; 3. Está relacionado con un cambio en la consistencia de las deposiciones. En cuanto a los requerimientos de duración de las molestias hay que tener en cuenta que los criterios deben cumplirse durante los últimos tres meses y los síntomas haber comenzado un mínimo de seis meses antes del diagnóstico2,3.
El solapamiento del SII con otros TFI (como el EF o la diarrea funcional), otros trastornos funcionales digestivos no intestinales (como la dispepsia funcional o la pirosis funcional) o extradigestivos (como la fibromialgia o la cistitis intersticial) es muy frecuente13,14.
El diagnóstico debe fundamentarse en los síntomas característicos que se han sistematizado en los criterios de Roma IV (Tabla 1, tabla 2, Fig. 2), aunque ello no exime de realizar las exploraciones pertinentes para establecer el diagnóstico diferencial con algunas patologías orgánicas que pueden manifestarse de forma similar.
3. ¿Qué es el síndrome del intestino irritable con estreñimiento?
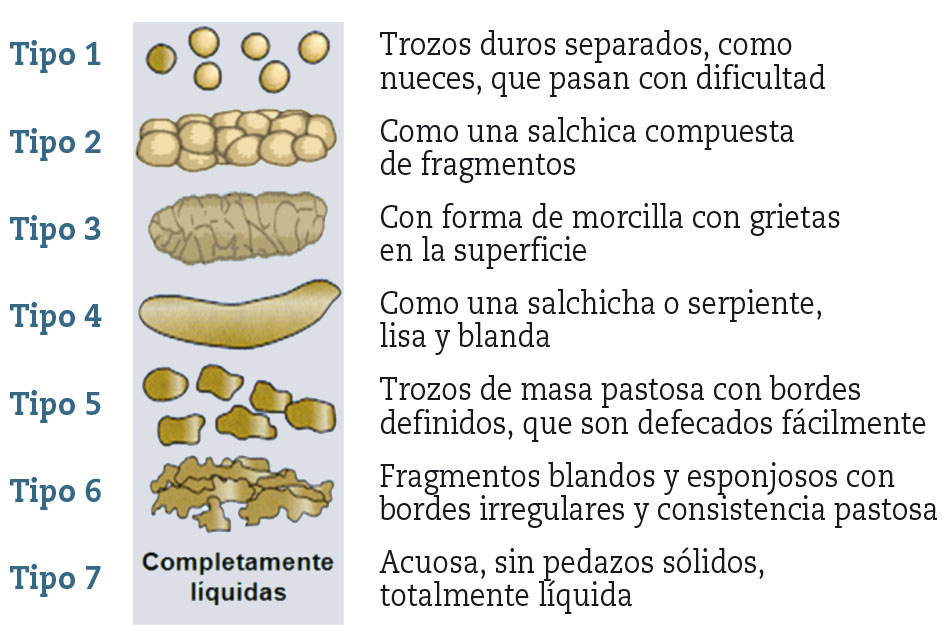
El SII-E es el subtipo de SII en el que el estreñimiento es la alteración deposicional predominante. Las características de las heces permiten clasificar los subtipos del SII utilizando la escala de Bristol (Fig. 3)15. Según el porcentaje de uno u otro tipo de heces, en los días en que estas son anormales, se establecen como SII- E, SII -D o SII -M. En el caso de SII-E se precisa que en más de un 25 % de las deposiciones las heces sean de tipo 1 o 2 y que en menos de un 25 % de las deposiciones las heces sean de tipo 6 o 72,3.
4. ¿Qué es el estreñimiento funcional?
El estreñimiento se caracteriza por la dificultad o la escasa frecuencia en relación con las deposiciones, a menudo acompañado por esfuerzo excesivo durante la defecación o sensación de evacuación incompleta2,3. En la mayoría de los casos no tiene una causa orgánica subyacente, siendo considerado un TFI. De acuerdo a los criterios de Roma IV el EF se define como la presencia durante los últimos 3 meses de dos o más de los siguientes: 1. Esfuerzo defecatorio (≥ 25 % deposiciones); 2. Deposiciones duras o caprinas (≥ 25 % deposiciones); 3. Sensación de evacuación incompleta (≥ 25 % deposiciones); 4. Obstrucción defecatoria (≥ 25 % deposiciones); 5. Maniobras manuales para la defecación (≥ 25 % deposiciones); y 6. Menos de 3 deposiciones espontáneas completas/semana. Los síntomas deben haber comenzado un mínimo de 6 meses antes del diagnóstico, no existir diarrea si no es tras la toma de laxantes, y no cumplirse criterios de SII2.
La Asociación Americana de Gastroenterología (AGA) prefiere realizar una definición más sencilla, aunque en realidad es muy similar: “Defecaciones insatisfactorias caracterizadas por deposiciones infrecuentes, heces difíciles de evacuar, o ambos, durante al menos 3 meses. La dificultad en evacuar las heces incluye el esfuerzo, la sensación de evacuación incompleta, las heces duras, el tiempo prolongado para defecar y la necesidad de maniobras manuales”16.
Sin embargo, estas definiciones han sido establecidas por consensos médicos y opiniones de expertos, siendo importante conocer cuál es la opinión de los propios pacientes sobre el estreñimiento. Así, en un estudio poblacional realizado en EE.UU., de un total de 557 sujetos con estreñimiento el porcentaje de síntomas que aquejaban eran los siguientes: 79 % esfuerzo excesivo, 74 % gases, 71 % heces duras, 62 % molestia abdominal, 57 % deposiciones poco frecuentes, 57 % distensión abdominal y 54 % sensación de evacuación incompleta17.
5. ¿En qué se parecen y en qué se diferencian el síndrome del intestino irritable con estreñimiento y el estreñimiento funcional?
Tal y como se ha comentado anteriormente son muchas las similitudes clínicas entre el SII-E y el EF: más frecuentes en personas de características similares (mujeres de mediana edad), obviamente la presencia de estreñimiento (pero también de distensión/hinchazón abdominal), y respuesta similar del estreñimiento a fármacos comunes. Además, es importante hacer constar que el estreñimiento es de características semejantes en ambos TFI4. La diferencia fundamental estriba en la presencia o ausencia de dolor, pero nuevamente se debe señalar que este es un aspecto discutible, y no evaluable como “todo o nada”.
En lo que se refiere a la fisiopatología, las causas del estreñimiento también son comunes: alteraciones de la motilidad colónica, dificultad expulsiva, ausencia de compresión abdominal suficiente, y combinación de las anteriores. Recordar, no obstante, que en un considerable número de casos (en especial con SII-E) puede no detectarse ninguna de las causas anteriores.
La diferencia fisiopatológica fundamental pudiera ser la distinta sensibilidad visceral en uno y otro caso: más frecuente la hipersensibilidad colónica en el SII y más frecuente la hiposensibilidad rectal en el EF18-20.
6. ¿Cuál es la importancia clínica, social y económica del síndrome del intestino irritable con estreñimiento y del estreñimiento funcional?
Algunos médicos consideran al SII-E y el EF como unas patologías banales pero la realidad es que su repercusión personal, sanitaria y social es muy importante. La calidad de vida relacionada con la salud (CVRS) de los pacientes con SII está notablemente alterada como reflejan varias revisiones al respecto21,22. A su vez, los costes asociados al SII son importantes. Baste citar que solo en los EE.UU. consultan anualmente por este problema 3,5 millones de personas, lo que supone un gasto anual de 20.000 millones de dólares23. Datos obtenidos en Europa, y específicamente en España, también demuestran el incremento de los costes directos e indirectos en los pacientes con SII-E24.
En lo que se refiere a la repercusión del EF en las actividades cotidianas de los pacientes que lo padecen, el 69 % considera que afecta a su rendimiento escolar o laboral17, siendo una causa relevante de absentismo en los casos graves (media de pérdida de días de actividad de 2,4/mes) y de disminución de la productividad17. Otros estudios han confirmado las repercusiones sociales al comparar datos de sujetos con EF y población general25. Todo ello condiciona que el gasto sanitario, directo e indirecto, del EF sea enorme. En EE.UU. conlleva aproximadamente 2,5 millones de visitas cada año y 92.000 hospitalizaciones anuales, con un coste en exploraciones de casi 7.000 millones de dólares25,26.
En lo que respecta a la CVRS en el EF sirvan como resumen los resultados de una revisión sistemática publicada en el año 2010. Se identificaron 10 estudios utilizando diferentes cuestionarios de salud genéricos: siete que utilizaban el SF-36 (Short Form 36), dos el PGWBI (Psychological General Well Being Index) y uno el SF-1227. Se comprobó que, utilizando el SF-36, prácticamente todos los dominios estaban alterados en los pacientes con EF al compararlos con los controles sanos; como era de esperar las diferencias eran mayores en los pacientes atendidos en el ámbito hospitalario que en el ambulatorio.
Cuando se compara la CVRS de los pacientes con estreñimiento con otras patologías frecuentes el resultado es sorprendente27. El impacto en los aspectos físicos de los pacientes con EF que precisan atención especializada es mayor, por ejemplo, que el de la colitis ulcerosa, estable o inestable, la enfermedad de Crohn estable, o que el de enfermedades no digestivas como las alergias crónicas, o el dolor de espalda.
7. ¿Cómo establecer la gravedad del síndrome del intestino irritable con estreñimiento y del estreñimiento funcional?
La gravedad de los TFI, incluidos el SII y el EF, depende no sólo de la intensidad de los síntomas intestinales sino también de otros factores biopsicosociales: asociación de síntomas gastrointestinales y extraintestinales, grado de afectación, y formas de percepción y comportamiento. De tal forma, tanto los factores fisiológicos viscerales como los centrales influyen en la gravedad del SII. A su vez, la gravedad, afecta directamente a la calidad de vida, y debe tenerse en cuenta a la hora de tomar decisiones diagnósticas y terapéuticas28,29.
La gravedad del SII, y de otros TFI, se establece por lo general de dos formas: 1) Utilizando una escala individual de síntomas (ej.: leve, moderado, grave, muy grave); o 2) Mediante la combinación de múltiples síntomas o actitudes (ej.: dolor abdominal junto con la consistencia y frecuencia de las deposiciones, urgencia defecatoria, impacto en la calidad de vida, utilización de recursos sanitarios, y grado de discapacidad).
El cuestionario más ampliamente utilizado para valorar la gravedad del SII es el llamado “Irritable Bowel Syndrome Severity Scoring System (IBS-SSS)»30. En él se analizan la intensidad de 5 ítems diferentes durante un periodo de 10 días: dolor abdominal, distensión, frecuencia de las deposiciones, consistencia de las deposiciones, e interferencia con las actividades cotidianas. Cada ítem se puntúa de 0 a 100 en una escala visual analógica, obteniéndose el sumatorio de las 5 puntuaciones. El IBS-SSS ha sido traducido y validado al español31.
Diagnóstico
8. ¿Cuántos tipos fisiopatológicos hay en el estreñimiento funcional (sin o con síndrome de intestino irritable)?
El EF se clasifica según los mecanismos fisiopatológicos implicados en tres grupos2,32-35.
- Pacientes con trastorno funcional de la defecación (Tabla 3)36: En los que se detecta una alteración del vaciado rectal ocasionado por una insuficiente propulsión rectal o por un comportamiento anómalo de la relajación de la musculatura estriada responsable de la apertura del canal anal (déficit de relajación, contracción paradójica o disinergia de la defecación). Ambas disfunciones pueden asociarse y a menudo se acompañan de una disminución de la sensibilidad rectal (hiposensibilidad), defectos estructurales del suelo pélvico (descenso perineal excesivo, rectocele, enterocele, intususcepción, etc.) o por trastornos de la motilidad colónica con retraso del tiempo de tránsito colónico (TTC)33.
- Pacientes con tránsito colónico lento (TCL), en los que el tiempo que tarda el material intestinal en recorrer el colon está aumentado con respecto a la normalidad.
- Pacientes con tránsito colónico normal (TCN).
El diagnóstico de estos subtipos fisiopatológicos precisa de técnicas diagnósticas funcionales complementarias que deben realizarse en centros especializados.
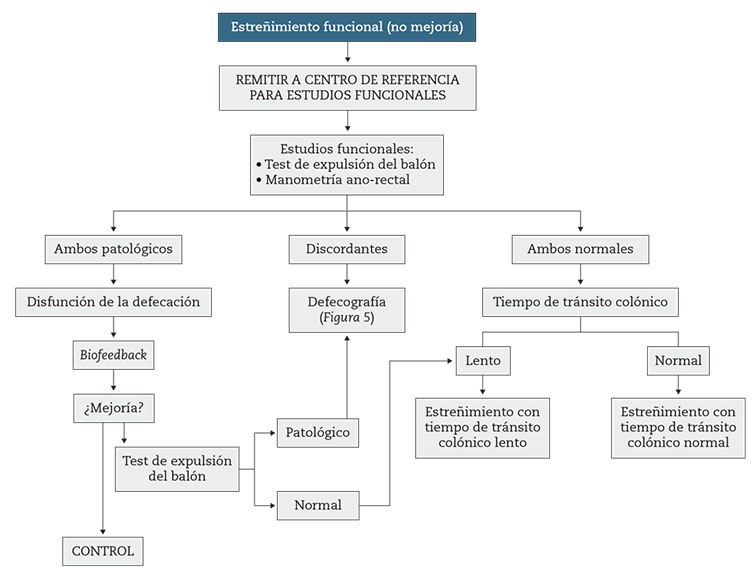
¿Qué estudios funcionales permiten establecer el diagnóstico de disfunción de la defecación, en qué orden y dónde deben realizarse?
Hay tres técnicas exploratorias que nos sirven para hacer el diagnóstico, y aunque no existe consenso que permita unificar la metodología de cada una de ellas, es necesario verificar mediante como mínimo dos técnicas la presencia de una evacuación ineficaz33.
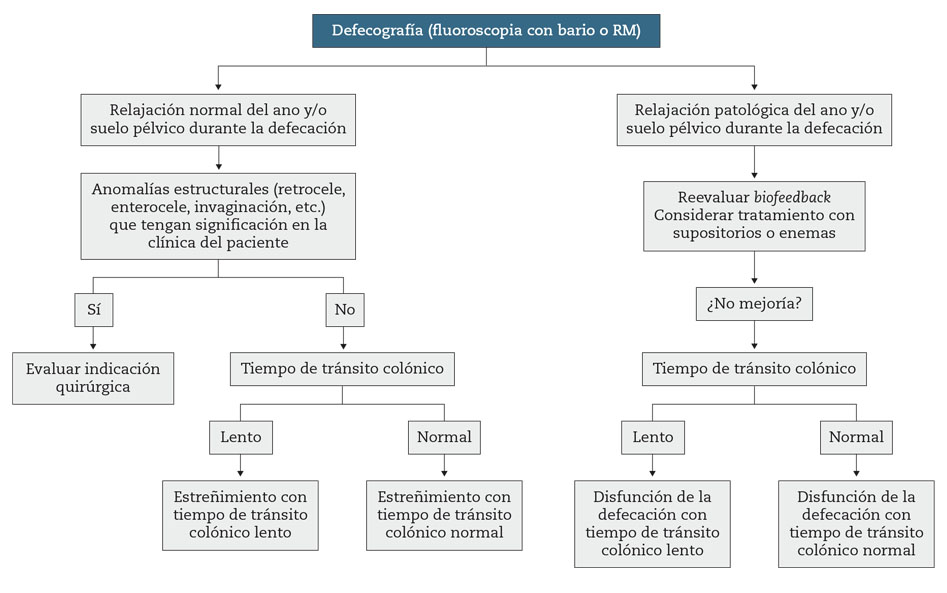
El test de expulsión del balón, por su accesibilidad, sencillez, coste, ausencia de efectos secundarios, sensibilidad y especificidad diagnóstica, deberá ser siempre el primero en realizarse33,35,37,38. Aunque no requiere un centro especializado, en la práctica clínica es muy difícil que en asistencia primaria o en consulta especializada ambulatoria se realice. Este test consiste en evaluar la habilidad de un paciente para expulsar, en condiciones de intimidad, un globo lleno de agua a temperatura corporal y con un volumen suficiente como para producir deseos de defecación. Se considera normal, la expulsión en un tiempo máximo de 1 a 2 minutos. En un estudio no controlado, en pacientes con EF se ha observado que esta prueba es útil para identificar disfunción de la defecación y muestra una sensibilidad y especificidad del 87,5 % y 89 %, respectivamente, y unos valores predictivos positivos y negativos del 64 % y 97 %, respectivamente39. La probabilidad por tanto de que un paciente presente un trastorno de la expulsión si el estudio es normal es muy baja, sin embargo, cuando es patológica deberemos realizar una cuantificación meticulosa de la función rectoanal que justifique esta alteración. El estudio más útil para ello es la manometría ano-rectal33,35,37,38, que registra, tanto en reposo como durante la maniobra defecatoria espontánea o provocada tras la distensión de un balón intrarrectal, las presiones a lo largo del canal anal y del recto, valora la sensibilidad rectal e identifica la indemnidad de los reflejos rectoanales. En los pacientes con disinergia se objetivará la inadecuada relajación o la contracción paradójica del canal anal y la presencia o no de una presión intrarrectal suficiente para propulsar las heces. Tanto el test de la expulsión del balón como la manometría ano-rectal, presentan entre otros, el inconveniente de que se hacen con el canal anal ocupado permanentemente por una sonda y ello no garantiza que la maniobra defecatoria reproduzca la situación que el individuo experimenta en la vida cotidiana. Por ello, en caso de que los síntomas del paciente no se justifiquen con los hallazgos en ambos estudios, o exista divergencia en el resultado de los mismos, deberemos realizar una defecografía34,40. Esta técnica, permite estudiar además de la función, la anatomía del recto-ano durante el acto voluntario de la defecación. Existen dos técnicas para su realización, la videofluoroscopia, en la que se evalúa y cuantifica la capacidad de expulsar el contenido rectal (con el paciente sentado en un asiento radiotraslúcido) y además la existencia de alteraciones estructurales del sigma, recto y canal anal y la defecografía con resonancia magnética (RM) que además visualiza los tejidos blandos perirrectales y el sistema génito-urinario en múltiples planos anatómicos, no utiliza radiación ionizante y es menos operador-dependiente que la videofluoroscopia. Ambas técnicas, deben hacerse en centros especializados y la interpretación de los resultados debe contrastarse siempre con los síntomas del paciente antes de tomar decisiones terapéuticas (sobre todo quirúrgicas), dada la alta prevalencia en sujetos normales de alteraciones morfológicas (rectocele, enterocele e intususcepción).
¿Qué estudios funcionales permiten establecer el diagnóstico de estreñimiento por tiempo de tránsito lento y dónde deben realizarse?
Existen tres técnicas que miden de forma cuantitativa el TTC total y en sus distintos segmentos: el estudio radiológico con marcadores radiopacos41, la evaluación gammagráfica del colon tras la ingesta de una comida42 o de una cápsula marcada con indio (111In-DTPA)43, y el estudio con cápsula inalámbrica de la motilidad (SmartPill®)44. Todas las técnicas deben realizarse e interpretarse en centros especializados, si bien por accesibilidad el estudio con marcadores radioopacos es el más ampliamente utilizado. En España, disponemos de un estudio con un número elevado de sujetos normales que nos proporciona valores de normalidad para los estudios radiológicos41. El uso de la SmartPill®, aunque de elevado coste, ha demostrado tener una buena correlación con los resultados de los estudios radiológicos para clasificar a los pacientes con TCL respecto a los de TCN, no es ionizante y mide además del tiempo la actividad motora en todo el tracto gastrointestinal. Este dato es muy importante cuando debemos decidir realizar cirugía exerética de colon en un paciente con TCL ya que previamente se deben descartar trastornos motores del resto del intestino.
9. ¿Qué utilidad clínica tiene conocer el tipo fisiopatológico de estreñimiento funcional?
Es muy útil en la práctica clínica hacer lo antes posible el diagnóstico de pacientes con disfunción de la defecación por disinergia del suelo pélvico, por su prevalencia, porque responden a tratamiento con biofeedback (BFB) pero no lo hacen a tratamiento habitual45-48 y además porque en un porcentaje elevado de pacientes la eficacia del BFB normaliza el TTC, cuando este estaba enlentecido45.
En pacientes sin disfunción de la defecación conocer el TTC nos va a permitir ser más o menos agresivos en la actitud terapéutica. Los pacientes con TCN no deberían nunca tratarse con medidas extremas y aún menos mediante cirugía. Por otra parte, los pacientes con TCL sin disfunción de la defecación frecuentemente presentan empeoramiento clínico al tratamiento con fibra y responderán mal a los laxantes habituales (incluyendo los estimulantes). En este subgrupo de pacientes, se ha demostrado que la neuromodulación de raíces sacras 49 y de forma muy selectiva la colectomía subtotal con anastomosis íleo-rectal pueden ser tratamientos eficaces y satisfactorios50,51.
10. ¿Puede un paciente presentar cambios en sus síntomas y cumplir en diferentes etapas de su vida ambos diagnósticos (síndrome del intestino irritable con estreñimiento y el estreñimiento funcional)?
Aplicando los criterios diagnósticos de Roma (especialmente con criterios previos a Roma IV) es muy frecuente tanto el solapamiento diagnóstico como el cambio de diagnóstico en el mismo individuo a lo largo del tiempo. Uno de los estudios prospectivos más importantes realizados en asistencia primaria demostró (n:432 pacientes; EF:231, SII-E:201), que el 89,5 % de pacientes con criterios de SII-E (tal y como eran definidos en 2005) cumplía así mismo criterios de EF y que el 43,8 % de pacientes con EF cumplían plenamente los criterios de SII-E, y además que el cambio en los diagnósticos en ambos sentidos (EF frente a SII-E y SII-E frente a EF) en un seguimiento de 12 meses se observaba hasta en un tercio de los pacientes52.
11. ¿Qué exploraciones complementarias son necesarias para el diagnóstico de síndrome del intestino irritable con estreñimiento y el estreñimiento funcional?
Como se ha comentado previamente, en la actualidad, el diagnóstico de SII-E y de EF se establecen mediante datos que se extraen de la historia clínica y que deben cumplir los criterios establecidos por consenso de grupos de expertos (Roma)3 (Tablas 1 y Tabla 2), o bien exclusivamente para EF, los criterios descritos previamente de la AGA32.
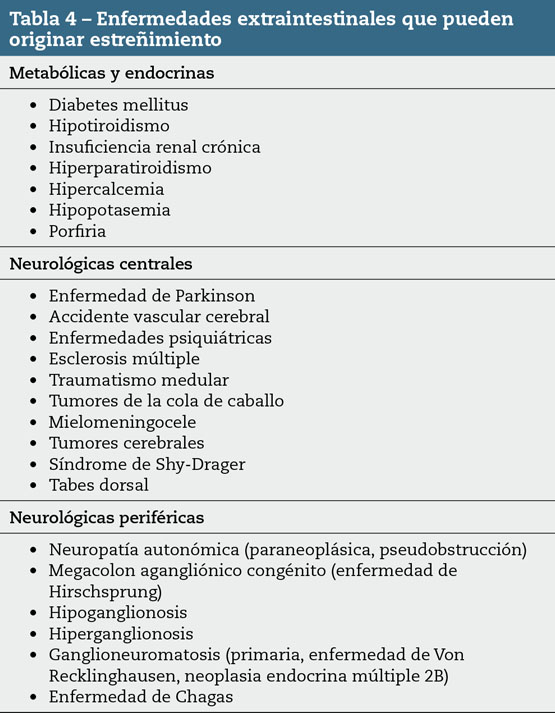
Una vez se constatan los criterios específicos que constituyen el diagnóstico de cualquiera de los dos procesos (SII-E y EF) y dado que es requisito imprescindible que el origen de los síntomas no tenga una justificación orgánica, metabólica ni farmacológica, debemos establecer criterios muy claros respecto a qué estudios complementarios son necesarios para garantizar la funcionalidad de los síntomas. La anamnesis dirigida y la exploración física rigurosa, son obligatorias y nos ayudan a confirmar la ausencia de enfermedades intestinales y extraintestinales (Tabla 4) o de la toma de fármacos (Tabla 5) que justifiquen los síntomas. Así mismo, nos permiten conocer si cumplen criterios de alarma (Tabla 6) que favorezcan la realización específica de determinados estudios complementarios.
En ausencia de criterios de alarma ¿qué estudios de laboratorio o de imagen se consideran imprescindibles para descartar causalidad metabólica u orgánica en pacientes que cumplen los criterios clínicos consensuados de SII-E o de EF?
A excepción de un hemograma para evaluar la existencia de anemia y/o infección, no se ha demostrado que la realización de estudios en los que se determinen electrolitos, hormonas tiroideas, calcio y perfil bioquímico completo (glucosa en ayunas, urea, creatinina, etc.) tengan utilidad diagnóstica ni sean costo-eficaces32,34,52. De forma que estas pruebas solo deben solicitarse cuando exista una sospecha específica de alguno de los trastornos anteriores.
Tampoco se ha demostrado que la realización de radiología simple de abdomen53,54 o de enema opaco55 tenga utilidad para encontrar características morfológicas que les discriminen respecto a la población normal y no hay ninguna evidencia que soporte la utilidad de la realización de colonoscopia en pacientes con clínica de estreñimiento56,57. Por ello, las guías de consenso32,34,40 no recomiendan realizar estudios de laboratorio ni morfológicos a excepción de que el médico observe criterios de riesgo o sospecha clínica de patología orgánica o metabólica.
¿Qué estudios debemos realizar si existen criterios de alarma?
Además de pedir las pruebas específicas en función del hallazgo guía de alarma, en la mayoría de casos deberá realizarse una colonoscopia.
¿Qué controles de laboratorio o de imagen debemos hacer a los pacientes cuyo diagnóstico de SII-E o de EF tenga varios años de evolución y se mantenga clínicamente estable sin signos ni síntomas de alarma?
Ninguno. La única excepción es cuando el paciente cumpla criterios poblacionales de cribado de cáncer colorrectal (CCR) por edad, o por la aparición en su entorno familiar de CCR. En estos casos deberán realizarse los estudios aplicables a cada caso: sangre oculta en heces (SOH) o colonoscopia34.
¿Qué controles debemos hacer en pacientes cuyo diagnóstico de SII-E o de EF esté bien establecido pero aparezcan cambios en la intensidad de los síntomas, en su frecuencia o en la respuesta al tratamiento?
En el supuesto de que no exista una explicación plausible para justificar los cambios, de forma individualizada se debe investigar la presencia de patología asociada que lo justifique. Es importante tener en consideración, tras una nueva exploración física, cuándo se realizaron los últimos estudios analíticos y morfológicos (si los tuviera) y si han cambiado las características epidemiológicas familiares. Característicamente, ambas patologías cursan con fases en las que hay cambios en la intensidad de los síntomas o en la percepción personal de que padecen una enfermedad orgánica no suficientemente investigada. Además, hay que tener en consideración que tanto el EF como el SII-E son diagnósticos intercambiables en el mismo individuo con el curso del tiempo si aplicamos los criterios diagnósticos de Roma, de manera que hasta un tercio de los pacientes con EF cumplirá criterios de SII-E en el seguimiento a un año y viceversa5 y ello no debe ser motivo de exploraciones complementarias. Únicamente síntomas o signos de alarma justifican el hacer estas.
Una vez diagnosticado a un paciente de SII-E o de EF ¿qué estudios funcionales deberíamos realizar y cuándo? ¿Son útiles los síntomas para sospechar el mecanismo patogénico por el que se produce el EF?
Los pacientes con estreñimiento, cumplan criterios o no de SII, pueden presentar alteraciones funcionales rectoanales, o trastornos de la motilidad del colon que no van a responder a medidas habituales por lo que es necesario un diagnóstico específico mediante estudios funcionales (Fig. 4 y Fig. 5). El trastorno funcional rectoanal más frecuente es la disfunción defecatoria por disinergia de la defecación, que afecta entre un 14,9 % y un 52,9 % de pacientes con EF38 y que consiste básicamente en una alteración de la apertura del ano en el momento de la defecación o en una insuficiente propulsión rectal en la fase expulsiva. El diagnóstico precoz de este trastorno es muy importante dado que precisa un tratamiento específico (BFB ano-rectal). Existen datos en la historia clínica, que aunque no son específicos para el diagnóstico de disinergia ano-rectal58,59, son más frecuentes en esta entidad, como se ha señalado en algunos estudios, como son el dolor anal con la defecación8, la ayuda manual para la expulsión de las heces, el esfuerzo excesivo para defecar y el bloqueo anal60. Además, hay un signo que se relaciona fuertemente con este trastorno cuando lo detectan profesionales experimentados, y es el hecho de objetivar una contracción paradójica del ano al invitar al paciente a efectuar una maniobra defecatoria durante la realización de un tacto ano-rectal61,62. Si el paciente presenta este signo, realizado por personal experto, y en condiciones de intimidad deberemos solicitar un test funcional de expulsión del balón y si este es patológico una manometría ano-rectal para confirmar el diagnóstico de disinergia. Sin embargo, y dado que en la práctica clínica estos requisitos (experiencia en tacto ano-rectal dinámico, áreas de exploración bien acondicionadas) no suelen darse, las guías de práctica clínica estiman que estas pruebas deben solicitarse ante cualquier paciente que no haya respondido a tratamiento con medidas higiénico-dietéticas, cambios en el estilo de vida y laxantes habituales y en el que por los síntomas o el tacto anal se sospeche la existencia de disinergia34,38; siendo más rigurosos, incluso puede exigirse antes de realizar estas exploraciones a los pacientes también refractarios a los tratamientos con agonistas de la serotonina y secretagogos40. En los pacientes en los que exista discordancia en los resultados del test de expulsión del balón y la manometría ano-rectal, se debe solicitar una defecografía mediante fluoroscopia o RM con el fin de evaluar la presencia de alteraciones estructurales ocultas (enterocele, intususcepción, rectocele) y/o confirmar la existencia de disfunción de la musculatura pelviana durante la maniobra de defecación.
Hay síntomas que en algunas series observacionales son más prevalentes en pacientes con EF con un TCL: la infrecuencia defecatoria60,63, el estreñimiento desde la infancia y la dependencia de los laxantes63, pero únicamente la consistencia de las heces (muy duras, escala de Bristol < 3) se ha objetivado que tiene un valor predictivo para el diagnóstico de TCL (sensibilidad 85 %, especificidad 82 %)64. En el momento actual el estudio del TTC se debe realizar en los pacientes que no responden a ninguna medida terapéutica y siempre después y aconsejando además descartar la existencia de disinergia ano-rectal mediante el estudio específico realizado mediante el test de expulsión del balón y la manometría ano-rectal32,34,40.
12. ¿Se puede, en una consulta de AP diagnosticar subtipos fisiopatológicos de estreñimiento funcional? ¿Cómo?
Por criterios diagnósticos, los subtipos fisiopatológicos de estreñimiento precisan de técnicas diagnósticas que no están accesibles en la consulta de AP, sin embargo, existen síntomas o signos exploratorios básicos que han demostrado tener una correlación bastante buena con los resultados de estas técnicas. Dada la importancia que podría tener desde el punto de vista pronóstico y fundamentalmente terapéutico priorizar en función de la sospecha estudios específicos, es muy importante conocer e identificar estos síntomas y signos.
Para poder efectuar una aproximación diagnóstica en AP de los diferentes subtipos de EF deberemos realizar una historia clínica y una exploración física minuciosas. En la anamnesis es trascendental conocer el patrón defecatorio habitual (frecuencia y consistencia de las heces), los síntomas y signos acompañantes (dolor, malestar, distensión abdominal, esfuerzo defecatorio, sensación de evacuación incompleta, manualización para defecar, etc.) así como los antecedentes personales de tratamientos previos (cambios de estilo de vida, cambios dietéticos, laxantes, fármacos analgésicos, antidepresivos, etc.) y la respuesta obtenida. La exploración física ha de incluir una exploración abdominal completa, una inspección anal y perineal y un tacto rectal dinámico (con maniobra defecatoria)65.
Con estos datos, como se ha comentado en el apartado anterior, se obtendrán síntomas que por su prevalencia en subtipos de EF sugieren la existencia de una disinergia de la defecación o de un TCL y fundamentalmente un signo (la disinergia anal durante el tacto ano-rectal) que tiene valor predictivo, en manos expertas, para el diagnóstico de disinergia de la defecación.
Figura 1
Figura 2 – Algoritmo diagnóstico del síndrome del intestino irritable con estreñimiento (SII-E) y del estreñimiento funcional (EF).
Figura 3 – Escala de Bristol (Traducido de: Lewis SJ, Heaton KW. Stool form scale as a useful guide to intestinal transit time. Scand J Gastroenterol. 1997; 32: 920-4).
Figura 4 – Algoritmo diagnóstico del estreñimiento funcional que no responde al tratamiento estándar y precisa de estudios funcionales.
Figura 5 – Algoritmo diagnóstico del estreñimiento funcional en los pacientes evaluados mediante defecografía para evaluar con mayor profundidad posibles alteraciones anatomo-funcionales.
Tratamiento
(Ver publicación 2ª parte; incluye preguntas 13-34).
Coordinación entre niveles asistenciales
35. ¿Cuándo se debe derivar a un paciente con síndrome del intestino irritable con estreñimiento o con estreñimiento funcional a una consulta especializada? Diagnóstico y coordinación entre niveles asistenciales
El diagnóstico del SII-E o del EF queda bien establecido en los criterios propuestos por el panel de expertos de Roma (Tabla 1 y tabla 2, Fig. 2, Fig. 4 y Fig. 5). Sin embargo, el profesional de AP siempre ha de tener presentes diferentes situaciones en las que ha de valorar la derivación a la atención especializada fundamentalmente para descartar organicidad pero también, en algunas ocasiones, para optimizar el seguimiento y el tratamiento de estos pacientes en el marco de una atención integrada y compartida. Para ello, resulta imprescindible una anamnesis adecuada incluyendo antecedentes familiares y personales, investigar la presencia de síntomas y signos de alarma y una exploración física minuciosa.
Diferentes documentos de consenso y GPC establecen diferentes motivos que obligan a descartar patología orgánica aunque la precisión diagnóstica de alguno de ellos es controvertida (Tabla 6).
También pueden ser motivo de derivación a una consulta especializada la presencia de síntomas persistentes o con mala respuesta al tratamiento, un deterioro importante de la calidad de vida, la no accesibilidad a pruebas diagnósticas o a dudas en el diagnóstico34,39,40,66-72.
36. ¿Cuándo se debe derivar a un paciente con SII-E o con EF, con diagnóstico de certeza a una consulta de gastroenterología o de otras especialidades?
En la actualidad, pueden existir vías de actuación diferentes en cada departamento o área asistencial, en función de la existencia o no de protocolos de actuación. Lo ideal, es crear unos sistemas de actuación por procedimientos según los cuales, el médico de AP tenga acceso directo al especialista de Digestivo con el fin de consultar cambios en el tratamiento o derivar al paciente para la realización de estudios complementarios o tratamientos específicos únicamente accesibles a asistencia especializada.
En este sentido, sería razonable la derivación del paciente en los siguientes supuestos (ver también Tabla 7):
- No respondedores o intolerantes a tratamiento con medidas básicas higiénico-dietéticas, cambios de estilo de vida y laxantes habituales incluyendo tratamiento de rescate con laxantes estimulantes (bisacodilo y picosulfato sódico). En el supuesto de que existan vías de acceso no presenciales, la prescripción de fármacos agonistas de la serotonina o secretagogos puede realizarse por el médico de atención primaria consensuando con el especialista el seguimiento. En los pacientes con SII-E se incluirán los no respondedores a tratamiento con espasmolíticos o con antidepresivos.
- Pacientes con una exploración ano-rectal en los que se sospeche la existencia de una disfunción de la defecación.
- Pacientes que con un control satisfactorio de los síntomas, experimenten un empeoramiento no justificable. En estos casos la derivación puede ser bien al especialista de digestivo o en función de síntomas o signos asociados a consultas específicas (endocrino, ginecología, cirugía, psiquiatría, etc.)
- Pacientes, cuyas características psicológicas, actitud frente a los síntomas o cuestionamiento en la búsqueda constante de la organicidad de sus molestias requieran el refuerzo de la opinión de un especialista.
Agradecimientos
Los autores agradecen la colaboración de los responsables de las cuatro Sociedades Científicas de las que forman parte, así como el trabajo de apoyo de Marién Castillo Sánchez, de Joaquín León Molina en la gestión bibliográfica y de José María Tenías en el soporte metodológico. También agradecen especialmente las sugerencias y comentarios de los siguientes revisores externos: Agustín Balboa Rodríguez, R. Manuel Devesa Muñiz, Higinio Flores Tirado, Juan Manuel Mendive Arbeloa, Xavier Puigdengolas Armengol, Mercedes Ricote Belinchón, Cecilio Santander Vaquero, Jordi Serra Pueyo, Carlos A. Siljeström Laredo, María José Soria de la Cruz.
Abreviaturas
- ADT: Antidepresivos tricíclicos.
- AEG: Asociación Española de Gastroenterología.
- AGA: Asociación Americana de Gastroenterología.
- AP: Atención Primaria.
- ARN: Ácido ribonucleico.
- BFB: Biofeedback.
- CCR: Cáncer colorrectal.
- CVRS: Calidad de Vida Relacionada con la Salud.
- EF: Estreñimiento (crónico) funcional.
- FODMAP: Dieta exenta de oligosacáridos, disacáridos, monosacáridos y polioles fermentables.
- GMPc: Guanosín monofosfato cíclico.
- GPC: Guía de Práctica Clínica.
- IC: Intervalo de confianza.
- ISRS: Inhibidores de la recaptación de serotonina.
- ISRSN: Inhibidores de la recaptación de la serotonina y noradrenalina.
- NNT: Número Necesario de pacientes a Tratar.
- OR: “Odds ratio”.
- PEG: Polietilenglicol.
- RM: Resonancia magnética.
- RR: Riesgo Relativo.
- SEMERGEN: Sociedad Española de Médicos de Atención Primaria.
- SEMFYC: Sociedad Española de Medicina de Familia y Comunitaria.
- SEMG: Sociedad Española de Médicos Generales y de Familia.
- SEPD: Sociedad Española de Patología Digestiva.
- SII: Síndrome del Intestino Irritable.
- SII-D: Síndrome del Intestino Irritable con (predomino de) diarrea.
- SII-E: Síndrome del Intestino Irritable con (predominio de) estreñimiento.
- SII-M: Síndrome del Intestino Irritable mixto.
- SOH: Sangre Oculta en Heces.
- TCL: Tránsito Colónico Lento.
- TFI: Trastornos Funcionales Intestinales.
- TCN: Tránsito Colónico Normal.
- TTC: Tiempo de Tránsito Colónico.
Conflicto de intereses
Los autores firmantes de esta Guía de Práctica Clínica (GPC) lo hacen en nombre de la Sociedad Española de Patología Digestiva (SEPD), la Sociedad Española de Medicina de Familia y Comunitaria (semFYC), la Sociedad Española de Médicos de Atención Primaria (SEMERGEN), la Sociedad Española de Médicos Generales y de Familia (SEMG) o como socios de la Asociación Española de Gastroenterología (AEG). Ni estas sociedades científicas ni ninguno de los integrantes del grupo de trabajo tienen vinculación alguna con las compañías que desarrollan los fármacos para las patologías abordadas en esta GPC. La SEPD, la semFYC, la SEMERGEN y la SEMG, así como los componentes del grupo pertenecientes a las mismas, no tienen intereses económicos en las compañías que han realizado la investigación y distribuyen medicamentos para estas patologías del aparato digestivo, si bien mantienen, tanto sociedades como integrantes del grupo, una sostenida relación con las mismas en la promoción de formación, investigación y mejora de la práctica clínica hacia la promoción de la salud digestiva. Finalmente, la SEPD, la semFYC, la SEMERGEN y la SEMG, así como los autores firmantes declaran que este trabajo ha recibido financiación de Almirall y Allergan, que ha carecido de cualquier tipo de influencia externa en el mismo y que ninguna tercera parte ha participado en la deliberación ni desarrollo del mismo ni ha conocido el contenido del texto final, antes de su publicación efectiva en la Revista Española de Enfermedades Digestivas y resto de órganos de expresión de cada sociedad participante.
Bibliografía
- Mearin F, Ciriza C, Minguez M, Rey E, Mascort JJ, Pena Tack J, Mueller-Lissner S, E, et al. Clinical Practice Guideline: Irritable bowel syndrome with constipation and functional constipation in the adult. Rev Esp Enferm Dig. 2016; 108: 332-63.
- Longstreth GF, Thompson WG, Chey WD, Houghton LA, Mearin F, Spiller RC. Functional bowel disorders. Gastroenterology. 2006; 130: 1480-91.
- Lacy BE, Mearin F, Chang L, Chey WD, Lembo AJ, Simren M, et al. Bowel disorders. Gastroenterology. 2016; 150: 1393-407.
- Rey E, Balboa A, Mearin F. Chronic constipation, irritable bowel syndrome with constipation and constipation with pain/discomfort: similarities and differences. Am J Gastroenterol. 2014; 109: 876-84.
- Wong RK, Palsson OS, Turner MJ, Levy RL, Feld AD, von Korff M, et al. Inability of the Rome III criteria to distinguish functional constipation from constipation-subtype irritable bowel syndrome. Am J Gastroenterol. 2010; 105: 2228-34.
- Bharucha AE, Locke GR, Zinsmeister AR, Seide BM, McKeon K, Schleck CD, et al. Differences between painless and painful constipation among community women. Am J Gastroenterol. 2006; 101: 604-12.
- Kamm MA, Muller-Lissner S, Talley NJ, Tack J, Boeckxstaens G, Minushkin ON, et al. Tegaserod for the treatment of chronic constipation: A randomized, double-blind, placebo-controlled multinational study. Am J Gastroenterol. 2005; 100: 362-72.
- Novick J, Miner P, Krause R, Glebas K, Bliesath H, Ligozio G, et al. A randomized, double-blind, placebo-controlled trial of tegaserod in female patients suffering from irritable bowel syndrome with constipation. Aliment Pharmacol Ther. 2002; 16: 1877-88.
- Johanson JF, Morton D, Geenen J, Ueno R. Multicenter, 4-week, double-blind, randomized, placebo-controlled trial of lubiprostone, a locally-acting type-2 chloride channel activator, in patients with chronic constipation. Am J Gastroenterol. 2008; 103: 170-7.
- Drossman DA, Chey WD, Johanson JF, Fass R, Scott C, Panas R, et al. Clinical trial: lubiprostone in patients with constipation-associated irritable bowel syndrome – results of two randomized, placebo-controlled studies. Aliment Pharmacol Ther. 2009; 29: 329-41.
- Lembo AJ, Schneier HA, Shiff SJ, Kurtz CB, MacDougall JE, Jia XD, et al. Two randomized trials of linaclotide for chronic constipation. N Engl J Med. 2011; 365: 527-36.
- Johnston JM, Kurtz CB, MacDougall JE, Lavins BJ, Currie MG, Fitch DA, et al. Linaclotide improves abdominal pain and bowel habits in a phase IIb study of patients with irritable bowel syndrome with constipation. Gastroenterology. 2010; 139: 1877-86.e2.
- Vandvik PO, Wilhelmsen I, Ihlebaek C, Farup PG. Comorbidity of irritable bowel syndrome in general practice: a striking feature with clinical implications. Aliment Pharmacol Ther. 2004; 20: 1195-203.
- Whitehead WE, Palsson OS, Levy RR, Feld AD, Turner M, Von Korff M. Comorbidity in irritable bowel syndrome. Am J Gastroenterol. 2007; 102: 2767-76.
- Lewis SJ, Heaton KW. Stool form scale as a useful guide to intestinal transit time. Scand J Gastroenterol. 1997; 32(9): 920-4.
- Bharucha AE, Wald AM. Anorectal disorders. Am J Gastroenterol. 2010; 105: 786-94.
- Johanson JF, Kralstein J. Chronic constipation: a survey of the patient perspective. Aliment Pharmacol Ther. 2007; 25: 599-608.
- Posserud I, Syrous A, Lindstrom L, Tack J, Abrahamsson H, Simren M. Altered rectal perception in irritable bowel syndrome is associated with symptom severity. Gastroenterology. 2007; 133: 1113-23.
- Ng C, Danta M, Kellow J, Badcock CA, Hansen R, Malcolm A. Attenuation of the colorectal tonic reflex in female patients with irritable bowel syndrome.Am J Physiol Gastrointest Liver Physiol. 2005; 289: G489-94.
- Burgell RE, Scott SM. Rectal hyposensitivity. J Neurogastroenterol Motil. 2012; 18: 373-84.
- El-Serag HB, Olden K, Bjorkman D. Health-related quality of life among persons with irritable bowel syndrome: a systematic review. Aliment Pharmacol Ther. 2002; 16: 1171-85.
- Mearin F, Perello A, Perona M. Quality of life in patients with irritable bowel syndrome. Gastroenterol Hepatol. 2004; 27(Suppl 3): 24-31.
- Everhart JE, Ruhl CE. Burden of digestive diseases in the United States Part II: Lower Gastrointestinal Diseases. Gastroenterology. 2009; 136: 741-54.
- Tack J, Stanghellini V, Mearin F, Yiannakou Y, Layer P, Coffin B, et al. Economic burden of moderate to severe irritable bowel syndrome with constipation in six European countries: a 12-month observational study. [En prensa]. 2016.
- Sun SX, DiBonaventura M, Purayidathil FW, Wagner J-S, Dabbous O, Mody R. Impact of chronic constipation on health-related quality of life, work productivity, and healthcare resource use: an analysis of the national health and wellness survey. Dig Dis Sci. 2011; 56: 2688-95.
- Dennison C, Prasad M, Lloyd A, Bhattacharyya SK, Dhawan R, Coyne K. The health-related quality of life and economic burden of constipation. Pharmacoeconomics. 2005; 23: 461-76.
- Belsey J, Greenfield S, Candy D, Geraint M. Systematic review: impact of constipation on quality of life in adults and children. Aliment Pharmacol Ther. 2010; 31: 938-49.
- Drossman DA, Chang L, Bellamy N, Gallo-Torres HE, Lembo A, Mearin F, et al. Severity in irritable bowel syndrome: A Rome Foundation working team report. Am J Gastroenterol. 2011; 106: 1749-59.
- Mearin F, Lacy BE. Diagnostic criteria in IBS: useful or not? Neurogastroenterol Motil. 2012; 24: 791-801.
- Francis CY, Morris J, Whorwell PJ. The irritable bowel severity scoring system: A simple method of monitoring irritable bowel syndrome and its progress. Aliment Pharmacol Ther. 1997; 11: 395-402.
- Almansa C, García R, Barceló M, Díaz-Rubio M, Rey E. Translation, cultural adaptation and validation of a Spanish version of the Irritable Bowel Syndrome Severity Score. Rev Esp Enferm Dig. 2011; 103: 612-8.
- Brandt LJ, Schoenfeld P, Prather CM, Quigley EMM, Schiller LR, Talley NJ, et al. Evidence-based position statement on the management of chronic constipation in North America. Am J Gastroenterol. 2005; 100(Suppl 1): S5-S21.
- Bharucha AE, Wald A, Enck P, Rao S. Functional anorectal disorders. Gastroenterology. 2006; 130: 1510-8.
- Bharucha AE, Dorn SD, Lembo A, Pressman A, American Gastroenterological A. American Gastroenterological Association medical position statement on constipation. Gastroenterology. 2013; 144: 211-7.
- Wald A, Bharucha AE, Cosman BC, Whitehead WE. ACG Clinical guideline: Management of benign anorectal disorders. Am J Gastroenterol. 2014; 109: 1141-57.
- Rao SS, Bharucha AE, Chiarioni G, Felt-Bersma R, Knowles C, Malcolm A, et al. Anorectal disorders. Gastroenterology. 2016; 150: 1430-42.e4.
- Rao SSC, Meduri K. What is necessary to diagnose constipation? Best Pract Res Clin Gastroenterol. 2011; 25: 127-40.
- Videlock EJ, Lembo A, Cremonini F. Diagnostic testing for dyssynergic defecation in chronic constipation: meta-analysis. Neurogastroenterol Motil. 2013; 25: 509-20
- Minguez M, Herreros B, Sanchiz V, Hernandez V, Almela P, Anon R, et al. Predictive value of the balloon expulsion test for excluding the diagnosis of pelvic floor dyssynergia in constipation. Gastroenterology. 2004; 126: 57-62.
- Tack J, Mueller-Lissner S, Stanghellini V, Boeckxstaens G, Kamm MA, Simren M, et al. Diagnosis and treatment of chronic constipation – a European perspective. Neurogastroenterol Motil. 2011; 23: 697-710.
- Spanish Group for the Study of Digestive Motility. Measurement of colonic transit time (total and segmental) with radiopaque markers. National reference values obtained in 192 healthy subjects. Gastroenterol Hepatol. 1998; 21: 71-5.
- Bonapace ES, Maurer AH, Davidoff S, Krevsky B, Fisher RS, Parkman HP. Whole gut transit scintigraphy in the clinical evaluation of patients with upper and lower gastrointestinal symptoms. Am J Gastroenterol. 2000; 95: 2838-47.
- Burton DD, Camilleri M, Mullan BP, Forstrom LA, Hung JC. Colonic transit scintigraphy labeled activated charcoal compared with ion exchange pellets. J Nucl Med. 1997; 38: 1807-10.
- Camilleri M, Thorne NK, Ringel Y, Hasler WL, Kuo B, Esfandyari T, et al. Wireless pH-motility capsule for colonic transit: prospective comparison with radiopaque markers in chronic constipation. Neurogastroenterol Motil. 2010; 22: 874-E233.
- Chiarioni G, Salandini L, Whitehead WE. Biofeedback benefits only patients with outlet dysfunction, not patients with isolated slow transit constipation. Gastroenterology. 2005; 129: 86-97.
- Chiarioni G, Whitehead WE, Pezza V, Morelli A, Bassotti G. Biofeedback is superior to laxatives for normal transit constipation due to pelvic floor dyssynergia. Gastroenterology. 2006; 130: 657-64.
- Rao SSC, Seaton K, Miller M, Brown K, Nygaard I, Stumbo P, et al. Randomized controlled trial of biofeedback, sham feedback, and standard therapy for dyssynergic defecation. Clin Gastroenterol Hepatol. 2007; 5: 331-8.
- Heymen S, Scarlett Y, Jones K, Ringel Y, Drossman D, Whitehead WE. Randomized, controlled trial shows biofeedback to be superior to alternative treatments for patients with pelvic floor dyssynergia-type constipation. Dis Colon Rectum. 2007; 50: 428-41.
- Kamm MA, Dudding TC, Melenhorst J, Jarrett M, Wang Z, Buntzen S, et al. Sacral nerve stimulation for intractable constipation. Gut. 2010; 59: 333-40.
- Arebi N, Kalli T, Howson W, Clark S, Norton C. Systematic review of abdominal surgery for chronic idiopathic constipation. Colorectal Dis. 2011; 13: 1335-43.
- Bove A, Bellini M, Battaglia E, Bocchini R, Gambaccini D, Bove V, et al. Consensus statement AIGO/SICCR diagnosis and treatment of chronic constipation and obstructed defecation (Part II: Treatment). World J Gastroenterol. 2012; 18: 4994-5013.
- Muller-Lissner SA, Kamm MA, Scarpignato C, Wald A. Myths and misconceptions about chronic constipation. Am J Gastroenterol. 2005; 100: 232-42.
- Moylan S, Armstrong J, Diaz-Saldano D, Saker M, Yerkes EB, Lindgren BW. Are Abdominal X-Rays a Reliable Way to Assess for Constipation? J Urol. 2010; 184: 1692-7.
- Pensabene L, Buonomo C, Fishman L, Chitkara D, Nurko S. Lack of utility of abdominal X-rays in the evaluation of children with constipation: comparison of different scoring methods. J Pediatr Gastroenterol Nutr. 2010; 51: 155-9.
- Patriquin H, Martelli H, Devroede G. Barium enema in chronic constipation – is it meaningful. Gastroenterology. 1978; 75: 619-22.
- Pepin C, Ladabaum U. The yield of lower endoscopy in patients with constipation: survey of a university hospital, a public county hospital, and a Veterans Administration medical center. Gastrointest Endosc. 2002; 56: 325-32.
- Gupta M, Holub J, Knigge K, Eisen G. Constipation is not associated with an increased rate of findings on colonoscopy: results from a national endoscopy consortium. Endoscopy. 2010; 42: 208-12.
- Mertz H, Naliboff B, Mayer EA. Symptoms and physiology in severe chronic constipation. Am J Gastroenterol. 1999; 94: 131-8.
- Eltringham MT, Khan U, Bain IM, Wooff DA, Mackie A, Jefferson E, et al. Functional defecation disorder as a clinical subgroup of chronic constipation: Analysis of symptoms and physiological parameters. Scand J Gastroenterol. 2008; 43: 262-9.
- Koch A, Voderholzer WA, Klauser AG, MullerLissner S. Symptoms in chronic constipation. Dis Colon Rectum. 1997; 40: 902-6.
- Orkin BA, Sinykin SB, Lloyd PC. The Digital Rectal Examination Scoring System (DRESS). Dis Colon Rectum. 2010; 53: 1656-60.
- Tantiphlachiva K, Rao P, Attaluri A, Rao SSC. Digital rectal examination is a useful tool for identifying patients with dyssynergia. Clin Gastroenterol Hepatol. 2010; 8: 955-60.
- Glia A, Lindberg G, Nilsson LH, Mihocsa L, Akerlund JE. Clinical value of symptom assessment in patients with constipation. Dis Colon Rectum. 1999; 42: 1401-8.
- Saad RJ, Rao SSC, Koch KL, Kuo B, Parkman HP, McCallum RW, et al. Do stool form and frequency correlate with whole-gut and colonic transit? Results from a multicenter study in constipated individuals and healthy controls. Am J Gastroenterol. 2010; 105: 403-11.
- Lam TJ, Felt-Bersma RJF. Clinical examination remains more important than anorectal function tests to identify treatable conditions in women with constipation. Int Urogynecol J. 2013; 24: 67-72.
- Mínguez M, Mora F, Más P, Garrigues V. Guía práctica de actuación diagnóstico-terapéutica en estreñimiento crónico. Valencia: Fundación Española de Aparato Digestivo; 2013.
- Fukudo S, Kaneko H, Akiho H, Inamori M, Endo Y, Okumura T, et al. Evidence-based clinical practice guidelines for irritable bowel syndrome. J Gastroenterol. 2015; 50: 11-30.
- Ford AC, Moayyedi P, Lacy BE, Lembo AJ, Saito YA, Schiller LR, et al. American College of Gastroenterology monograph on the management of irritable bowel syndrome and chronic idiopathic constipation. Am J Gastroenterol. 2014; 109: S2-S26.
- Chey WD, Kurlander J, Eswaran S. Irritable bowel syndrome A Clinical Review. JAMA. 2015; 313: 949-58.
- Grupo de trabajo de la guía de práctica clínica sobre el síndrome del intestino irritable. Manejo del paciente con síndrome del intestino irritable. Barcelona: Asociación Española de Gastroenterología, Sociedad Española de Familia y Comunitaria y Centro Cochrane Iberoamericano; 2005.
- Serra J, Mascort-Roca J, Marzo-Castillejo M, Delgado Aros S, Ferrandiz Santos J, Rey Diaz Rubio E, et al. Clinical practice guidelines for the management of constipation in adults. Part 1: Definition, aetiology and clinical manifestations. Gastroenterol Hepatol. 2016 [En prensa]. doi: 10.1016/j.gastrohep.2016.02.006.
- Serra J, Mascort-Roca J, Marzo-Castillejo M, Aros SD, Ferrandiz Santos J, Rey Diaz Rubio E, et al. Clinical practice guidelines for the management of constipation in adults. Part 2: Diagnosis and treatment. Gastroenterol Hepatol. 2016 [En prensa]. doi: 10.1016/j.gastrohep.2016.02.007.
- Mearin F, Ciriza C, Mínguez M, Rey E, Mascort JJ, Peña E, et al. Guía de práctica clínica: síndrome del intestino irritable con estreñimiento y estreñimiento funcional en adultos: concepto, diagnóstico y continuidad asistencial. (Parte 1 de 2). Aten Primaria. 2017; 49: 42-55
- Mearin F, Ciriza C, Mínguez M, Rey E, Mascort JJ, Peña E, et al. Guía de práctica clínica: síndrome del intestino irritable con estreñimiento y estreñimiento funcional en adultos: concepto, diagnóstico y continuidad asistencial. (parte 1 de 2). Semergen. 2017; 43: 43-56.