Clínica Cotidiana
Información del artículo
Historia del artículo:
Recibido el 24 de agosto de 2020
Aceptado el 27 de noviembre de 2020
On-line el 9 de marzo de 2021
Palabras clave:
Enfermedad autoinmune
Etiología
Úlcera crónica
Úlcera atípica
*Autor para correspondencia
Correo electrónico:
mfesan@hotmail.com
(M.F. Sánchez Flores).
Keywords:
Autoimmune disease
Etiology
Chronic ulcer
Atypical ulcer
María Fe Sánchez Floresa, Ismael Calcerrada Alisesb, Mario Cañada Sánchezc, Pilar Nieto Gonzálezd
aCS Pisuerga. Arroyo de la Encomienda (Valladolid). bCS Medina del Campo Urbano. Medina del Campo (Valladolid). cCS Tórtola. Valladolid. dCS Medina del Campo Urbano. Medina del Campo (Valladolid).
Resumen
Múltiples procesos favorecen la aparición de úlceras en las extremidades inferiores; su diagnóstico clínico, a menudo, no es sencillo. Cuando la úlcera es atípica o de evolución tórpida debemos de considerar la posibilidad diagnóstica de enfermedades raras, en especial en pacientes jóvenes.
En este caso mostramos cómo algunas lesiones cutáneas cronificadas son de difícil abordaje si no se tienen en cuenta otras posibles causas aparte del origen vascular o neuropático. Nuestra finalidad es contribuir a la evaluación y abordaje de esta patología y colaborar en la formación de los profesionales de atención primaria implicados en el proceso de atención del paciente con úlceras crónicas.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Skin lesions of uncertain origin and torpid evolution
Abstract
Multiple processes promote the appearance of ulcers in the lower extremities and their clinical diagnosis is often not easy. When ulcer is atypical or odd evolution, we should consider the diagnostic possibility of rare diseases, especially in young patients.
In this case, we show how some skin lesions have a difficult approach if other possible causes are not taken into account other than the vascular or neuropathic origin of chronic ulcers. Our purpose is to contribute to the evaluation and approach of this pathology and to collaborate in the training of primary care professionals involved in the process of patient care with chronic ulcers.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Mujer de 37 años de edad, que acude a Urgencias por la aparición de un nódulo en la pierna y celulitis de un día de evolución, por probable picadura de insecto
Refiere no haber sufrido traumatismo previo; no tiene síntomas generales acompañantes. Antecedentes: sedentarismo, obesidad, enfermedad de Raynaud; flebectomía en la pierna derecha.
Es pescadera en un supermercado. Utiliza medias de compresión fuerte para su trabajo.
Durante la exploración general sus constantes vitales son normales, la glucemia posprandial es 124 mg/dl.
Transcurridos dos días en tratamiento con antibiótico (amoxicilina-clavulánico 500 mg/12 horas) y antiinflamatorio oral (ibuprofeno 600 mg/8 horas), presenta necrosis seca de 2 cm de diámetro en la extremidad inferior izquierda, dolorosa al tacto, que le produce sensación de quemazón/prurito con eritema perilesional y edema hasta la rodilla.
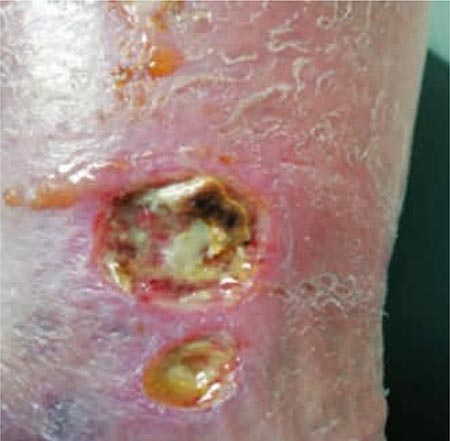
Se realiza desbridamiento cortante de la escara y posterior aplicación de hidrofibra plata (Acuacel plata) para descarga bacteriana1. Se aplica permanganato potásico al 1/10.000 para el eritema descamativo perilesional2. Se coloca vendaje de tracción corta de una sola capa. Tras cinco días de descarga bacteriana y antibiótico oral, se aprecia lecho de la herida de mayor tamaño con esfacelos, se desbrida mecánicamente y se aplica hidrogel (purilon) e hidrofibra (Acuacel extra) cura húmeda3. A los dos días la lesión tiene mayor superficie y profundidad, el lecho se vuelve fibrinoso, con esfacelos periféricos y mal olor. Se toma muestra para cultivo. Aparecen lesiones satélites de características similares (Fig. 1).
Se formula una segunda hipótesis de úlcera vascular de etiología mixta. Se aumenta a doble capa la compresión del vendaje y se trata lo que se considera infección con otra tanda de antibiótico oral y con pomada de betametasona al 0,5 % en los bordes, desbridamiento cortante y distintos apósitos desbridantes enzimáticos, así como medidas de proactividad física necesarias para que la paciente active la circulación arteriolar y venosa: limitar las bipedestaciones prolongadas; evitar el sedentarismo e incentivar la deambulación; reposo en horizontal con la pierna lesionada elevada, al menos, a 5-10 cm, durante 30 minutos y 2 veces al día.
Transcurridos 30 días y con mala evolución, se solicita analítica general con serología para Rickettsia, VIH, hepatitis, anticuerpos antifosfolípido, autoanticuerpos, cultivo de la herida para hongos, micobacterias y placa de tórax para descartar enfermedad sistémica. Todas las pruebas son negativas.
Figura 1
La paciente es remitida a Dermatología para completar el estudio, con la sospecha de pioderma gangrenoso (PG)4 (Fig. 2).
Con esta nueva hipótesis se modifica el procedimiento de cura con un enfoque radical, pues el objetivo del tratamiento consiste en reducir el proceso inflamatorio subyacente, reducir el dolor y proporcionar cuidados a la herida para favorecer la curación con mínimos efectos adversos6.
Se comienzan a tratar los bordes eritematosos no como una infección asociada a componente vascular (como se había hecho hasta ese momento), sino como un proceso inflamatorio. Desde ese momento se trata de estabilizar la fase inflamatoria de los bordes con cremas de corticoides y facilitar el retorno venoso y la microcirculación con vendaje de tracción corta, así como motivar a la paciente a realizar medidas proactivas que mejoren la perfusión tisular.
El intervalo de curas se establece cada 72 horas. Se utilizan apósitos que permiten 2 curas semanales y un vendaje que resista en buenas condiciones durante todo ese lapso.
Transcurridos tres meses, es estudiada en el hospital. Tras estudios analíticos, microbiológicos, anatomopatológicos y de imagen, se llega a la misma conclusión: PG.
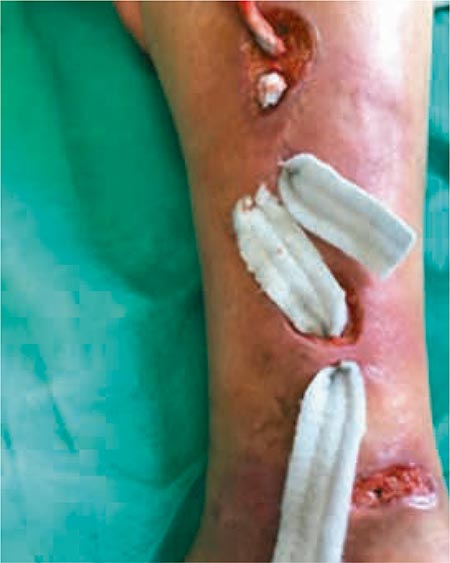
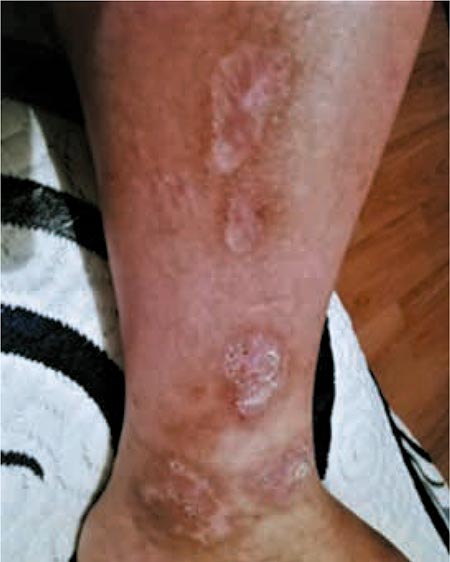
Es tratada con inmunosupresores orales (corticoides) y se mantienen las curas hasta su resolución (más de nueve meses). Las lesiones sufren tunelización que requiere una limpieza exhaustiva dolorosa (Fig. 3). Durante este tiempo es sometida a flebectomía del territorio afectado. Transcurridos unos nueve meses se consigue la resolución del caso, que deja como secuela tejido cicatricial (Fig. 4).
Figura 2 – Algoritmo de actuación para el pioderma gangrenoso.
Figura 3 –
Figura 4 –
Comentario
El PG es una enfermedad cutánea inflamatoria poco frecuente, de probable patogenia inmunitaria. Se caracteriza por la aparición de úlceras cutáneas de carácter necrótico que, sin un tratamiento adecuado, suelen tener una evolución tórpida, crónica y generalmente destructiva, con extensión a grandes superficies.
El diagnóstico diferencial del PG con otras patologías más frecuentes que cursan con úlceras es importante, ya que las curas y cuidados locales de las lesiones no suelen ser suficientes para el control de esta enfermedad. Suele precisar de un tratamiento sistémico adecuado para evitar su progresión y las secuelas del paciente, así como descartar otras enfermedades sistémicas autoinmunes asociadas5.
Alrededor del 1-2 % de la población mundial sufrirá úlceras en algún momento de su vida; su incidencia aumenta con la edad7,8. La cronicidad y recidiva de las heridas en las extremidades inferiores implica importantes costes directos e indirectos. La demora en el diagnóstico etiológico y sus implicaciones terapéuticas contribuyen a esta cronicidad.
Conocer las diferentes etiopatogenias es clave para poder establecer el diagnóstico diferencial entre ellas, ya que la etiología de las úlceras en las extremidades inferiores es multifactorial; un 75-80 % corresponden a etiología venosa9,10.
El correcto diagnóstico etiológico implica una buena anamnesis clínica y semiológica de la herida, así como evaluar el contexto local en que se desarrolla.
Habiendo escasa bibliografía disponible sobre casos clínicos difíciles, describimos este para poner de relieve las dificultades diagnósticas que ha implicado y las distintas fases del tratamiento hasta su resolución.
Existe un gran debate sobre la demora en los plazos de derivación desde atención primaria a atención hospitalaria, y cómo esta puede llegar a enlentecer la dinámica del proceso de curación de las heridas complejas. En nuestro caso, la espera por una interconsulta con el hospital motivó en la paciente una sensación de desamparo y alarma al no mejorar la lesión pese al tratamiento que se le aplicaba.
Conclusiones
Es necesaria una adecuada anamnesis para el diagnóstico correcto y la resolución de los casos de heridas complejas. Una coordinación multidisciplinar ágil permite un abordaje de las heridas complejas mucho más eficaz y eficiente para todos.
Las dilaciones de los procesos por un deficiente funcionamiento de los recursos pueden generar en paciente y profesionales sensaciones de rabia e impotencia. En consecuencia, dan lugar a tratamientos largos, inadecuados y costosos, que pueden afectar a la seguridad del paciente, disminuir de forma importante la calidad de vida de la persona y mermar la calidad asistencial que todo ello implica.
Puntos clave
- No todas las úlceras cronificadas tienen un origen exclusivamente vascular: se debe pensar en enfermedades no tan frecuentes.
- El abordaje compartido médico de familia y enfermería es fundamental para replantearse nuevos diagnósticos diferenciales.
- Ha de atenderse al paciente de manera integral, sin olvidar la esfera emocional, que suele alterarse ante procesos tórpidos cutáneos.
- Una buena gestión de los plazos de derivación mejora la eficacia y reduce enormemente los costes.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Blasco-García MC, Cuñarro-Alonso JM, Rueda-López J, Segovia-Gómez T, Delgado-Fernández R. Materiales y productos para la cicactrización de las heridas crónicas. En: García-Fernández FP, Soldevilla-Agreda JJ, Torra Bou JE (eds). Atención integral de las heridas crónicas. 2ª ed. Logroño: GNEAUPP-FSJJ; 2016. p. 503-30.
- Using potassium permanganate for wound cleansing. Readers’ Questions. J Wound Care.1994; 3: 4.
- Rodríguez M, Almozara R, García F, Malla R, Rivera J. Cuidados de enfermería al paciente con úlceras por presión. Guía de prevención y tratamiento. Cádiz: Hospital Universitario Puerta del Mar. 2003. Disponible en: http://www.aecut.es/index.php/descargas/doc_download/2-guia-del-hospitaluniversitario-puerta-del-mar-cadiz
- Maverakis E, Ma C, Shinkai K, Fiorentino D, Callen JP, Wollina U, et al. Diagnostic criteria of ulcerative pyoderma gangrenosum: A Delphi Consensus of International Experts. JAMA Dermatol. 2018; 154: 461-6.
- Wolff K, Johnson RA, Fitzpatrick K. Atlas en color y sinopsis de Dermatología Clínica. 6ª ed. Madrid: Médica Panamericana; 2010.
- Hernández Orta MP, Pina García R, Garbayo Ágreda Y, Martín de Aguilera Moro MC, Pérez Pelegay J, Lafuente Urrez RF, et al. Fuerte deterioro de la integridad cutánea por pioderma gangrenoso. Enfermería Dermatol. 2013; 20: 61.
- Capillas Pérez RM, Castillo Muñoz L, Morros Torné C, Portas Freixes J, Vedia Urgell C. Maneig de les úlceres vasculars. Barcelona:Institut Català de la Salut, 2004. Guies de pràctica clínica i material docent, Nº 10. Disponible en: http://docplayer.es/11877929-Maneig-de-les-ulceres-vasculars-direccio-clinica-en-l-atencio-primaria-guies-de-practica-clinica-i-material-docent-www-gencat.html
- Andersen CA, Aung BJ, Chandy RM, Doucette M, Garcia A, Garoufalis MG, et al. Improving the standard of care for treating venous leg ulcers within the Veterans Administration. Wounds [Online]. 2012; Suppl 1: 1-8.
- Gonsalves CF. Venous leg ulcers. Tech Vasc Interv Radiol. 2003; 6: 132-6.
- Grey JE, Harding KG, Enoch S. Venous and arterial leg ulcers. BMJ. 2006; 332: 347-50.