Artículo de Revisión
Información del artículo
Historia del artículo:
Recibido el 7 de abril de 2016
Aceptado el 14 de febrero de 2017
On-line el 26 de junio de 2017
Palabras clave:
Arbovirus
Dengue
Chikungunya
Zika
*Autor para correspondencia
Correo electrónico:
easanchezv@gmail.com
(E.A. Sánchez-Valdivieso).
Keywords:
Arboviruses
Dengue
Chikungunya
Zika
Armando Herrera Mayora, Enrique A. Sánchez-Valdivieso*
Departamento de Investigación. Universidad Cristóbal Colón. Boca del Río, Veracruz. México.
Resumen
Los arbovirus (virus transmitidos por artrópodos) constituyen problemas de Salud Pública muy importantes, dado el surgimiento prácticamente global de enfermedades arbovirales. Estas enfermedades se han extendido sin precedente en asociación con factores como la actividad humana y la tasa de recombinación viral, lo que favorece que vector y huésped interactúen, unido al comercio y a los viajes aéreos intercontinentales.
Los arbovirus han surgido en nuevas regiones del mundo debido a cepas con mayor adaptabilidad. Estas enfermedades se diagnostican en viajeros que regresan de países tropicales. El clima es factor importante en la determinación de la distribución geográfica y la eficiencia con la que estos virus se transmiten
Se pueden producir brotes epidémicos de inmensas proporciones con los efectos del cambio climático.
Esta amenaza puede ser mitigada con mejora de los programas de prevención y control, el fortalecimiento de aspectos de bioseguridad, vigilancia y pronta respuesta a los brotes y la colaboración intersectorial.
© 2017 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Emerging acute febrile arthropod-borne diseases: Dengue, Chikungunya and Zika
Abstract
Arboviruses (Arthropod-borne viruses) constitute significant Public Health problems, with the global re-emergence of arboviral diseases. These diseases have spread unprecedentedly associated with factors such as viral recombination rate and human activities, a closer vector-host interaction, and increased commerce and intercontinental air travel.
Arboviruses have emerged in new regions of the world, due to more adaptive strains. These acquired diseases are diagnosed in travellers returning from tropical countries. Climate is a major factor in determining the geographic distribution of arthropods and the efficiency with which they are transmitted.
© 2017 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Introducción
Las arbovirosis son generalmente enfermedades febriles agudas de áreas tropicales y subtropicales. Al menos 2.500 millones de personas viven en áreas de alto riesgo, por lo que estas enfermedades representan un importante problema de Salud Pública, ya que causan grandes epidemias y originan grandes gastos financieros relacionados con diagnóstico y tratamiento.
El diagnóstico de enfermedades arbovirales puede ser difícil debido a una similitud clínica con otras enfermedades, aparición oligosintomática, difícil acceso a laboratorios de referencia y reacciones cruzadas filogenéticas, especialmente en regiones endémicas.
Dengue
Constituye uno de los mayores retos de Salud Pública, ya que un 40 % de la población mundial corre riesgo de padecer esta enfermedad 1-3. El agente de esta enfermedad (DENV) es un flavivirus2,4,5. La transmisión se produce a través de la picadura de la hembra del mosquito Aedes aegypti (así como de A. albopictus)2,4,5-8.
El mosquito A. aegypti se alimenta de día preferentemente2; su actividad es amplia por la mañana y por la tarde6. Es endofágico (preferente por alimentarse dentro de los hogares) 9 y está presente en regiones tropicales.
El virus toma entre 8 y 12 días después de infectar al mosquito, antes de poder ser transmitido por él. Existe transmisión transovárica, que produce mosquitos que nacen ya infectados10. Los humanos tienen un periodo de latencia de 5 días para desarrollar la enfermedad (Fig. 1) y permanecen infectantes durante una semana6.
El cambio climático tiene un gran impacto en el dengue1,6,7,10-12. El mayor efecto está asociado con la temperatura mínima mensual, pues los mosquitos tienen preferencia por temperaturas más elevadas y buen nivel de humedad relativa7. Otro factor es la aparición de áreas urbanas con mínima vegetación y grandes superficies que absorben e irradian calor durante el día, las llamadas islas urbanas. Producen un aumento de la temperatura (hasta 30 °C o más) con bajas fluctuaciones durante el día, lo que aumenta la capacidad de replicación del virus, acelera el metabolismo del mosquito y reduce el período de diseminación a menos de 7 días13.
Entre los factores sociales que contribuyen a la diseminación del dengue se encuentra la densidad de población de moderada a alta, viviendas con desagües obstruidos, agua almacenada, ausencia de abastecimiento de agua corriente, disponibilidad intermitente de agua, el uso de depósitos destapados, y mal estado socioeconómico1,2,7,11,14-19.
Para diagnosticar el dengue existen métodos indirectos, como el hemograma y la detección de niveles de IgG e IgM2,4,12,20,21; la segunda es detectada a partir del sexto día y la primera a partir del decimocuarto día (Fig. 1)22, con la desventaja de la reactividad cruzada4 con otras clases de flavivirus12 y la necesidad de una segunda muestra confirmatoria20,21. Se ha popularizado la búsqueda de proteína no estructural 1 (NS1-ELISA)2,12,20; igualmente el aislamiento viral, considerado como el estándar de oro4, pero limitado por el corto periodo de viremia (5 días aproximadamente)4,22 y el período mínimo de 21 días para su desarrollo; y el uso de técnicas moleculares, rápidas, sensibles, específicas, reproducibles y automatizadas4, como la RT-PCR12,22 o las llamadas pruebas rápidas20. Las formas complicadas de la infección y sus consecuencias potencialmente fatales hacen considerar útil la confirmación para detectar inicio de epidemias y descartar diagnósticos diferenciales en periodos interepidémicos21.
Los factores de riesgo asociados a dengue grave son:
- Factores genéticos del virus y del huésped que modifiquen su virulencia.
- La ascendencia africana se asocia a protección contra las formas graves de la enfermedad.
- El sexo femenino, la edad de 45-69 años y la temporada de lluvias están relacionados con la presencia de enfermedad grave.
- Grupos de riesgo especialmente vulnerables a la infección son niños, neonatos, mujeres embarazadas y hepatópatas crónicos por hepatitis C.
- Circulación ambiental de distintos serotipos del DENV: zonas hiperendémicas con gran población de vector y durante la temporada de lluvias.
- El dengue serotipo DENV-2 seguido de DENV-3 se asocia a las formas graves de la enfermedad; el DENV-2 genotipo asiático se ha relacionado con una mayor proporción de complicaciones, a diferencia del genotipo americano.
- Infecciones previas que generen reacción cruzada mediante anticuerpos tipo IgG heterólogos (mecanismo de “ampliación dependiente de anticuerpos”, antibody dependent enhancement, –ADE–), lo que aumenta la viremia en la infección secundaria.
- El aumento descontrolado de citocinas proinflamatorias, como el TNF-alfa, aumenta la fragilidad endotelial y la fuga de líquido; aunque es común en las formas de dengue grave, no es el único mecanismo asociado.
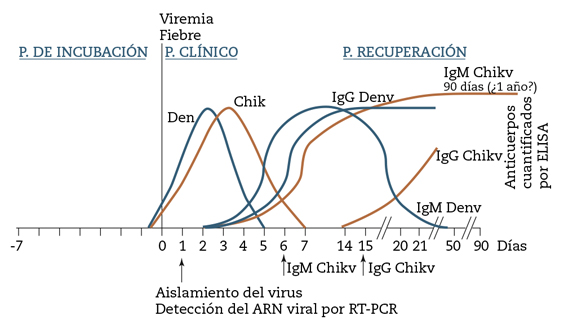
Figura 1 – Curvas de expresión de viremia y anticuerpos en Dengue y Chikungunya.
Virus Chikungunya (CHIKV)
También se transmite por los vectores A. aegypti y A. albopictus4,5,6,23,24, de la familia Togaviridae (género Alfavirus)24, que ha producido grandes brotes recientes y alta tasa de casos sintomáticos con complicaciones inesperadas y transmisión materno-infantil4.
Ocasiona una enfermedad con una tasa de mortalidad baja y síntomas similares al dengue, pero con mayor dolor articular. Recientemente sufrió una mutación que le hace ser transmitido de manera más efectiva, con un periodo de 2 a 6 días (CHIKV-R), a diferencia de su cepa clásica, con una incubación de 7 a 15 días (CHIKV-A), lo que le convierte en una cepa de preocupación epidemiológica por su mayor capacidad para generar epidemias5.
CHIK y dengue son enfermedades agudas caracterizadas por fiebre, mialgia y letargia. Algunos pacientes pueden tener también rash máculo-papular, náuseas, vómitos y cefalea. Distinguir los hallazgos de CHIK incluye poliartralgia bilateral debilitante y, en algunos casos, artritis.
Durante los primeros 5 días de la enfermedad deberá ser practicada la RT-PCR para detectar directamente ácido nucleico de CHIKV o de DENV en suero de casos sospechosos. Los especímenes de suero colectado 5 o más días después del inicio de los síntomas deberán ser evaluados para IgM anti-CHIKV y anti-DENV por inmunoensayo. Si los resultados iniciales resultan negativos pero aún se sospecha dengue o CHIK, debe colectarse suero 7 o más días después del inicio de la enfermedad y repetirse el análisis para detectar IgM.
El CHIK es rara vez mortal. En contraste, la identificación temprana y el abordaje clínico adecuado de los casos hospitalizados por dengue pueden reducir la tasa de casos fatales de 10 % a menos de 0,1 %. Por ello, los pacientes con sospecha de tener dengue o CHIK deben ser tratados como si tuvieran dengue (Tabla 1) hasta que esta enfermedad pueda ser descartada.
Los pacientes deben ser evaluados buscando presencia de signos de alarma de dengue grave (vómitos persistentes, dolor abdominal intenso, por ejemplo); si estuviesen presentes, deben ser hospitalizados para monitorización estrecha y seguimiento. La mayoría de los que desarrollan dengue grave lo hacen 24-48 horas después de la efervescencia y esto puede ocurrir rápidamente mientras el paciente está lúcido. El estado hemodinámico deberá ser mantenido con líquidos intravenosos isotónicos. El dolor y la fiebre en pacientes con sospecha de dengue o CHIK deberán ser tratados con paracetamol. No deben administrarse aspirina u otros antiinflamatorios no esteroideos (AINE) a dichos pacientes por el riesgo incrementado de manifestaciones hemorrágicas si el paciente tuviera dengue.
Virus Zika
La fiebre Zika es una enfermedad viral transmitida por los mismos mosquitos y causada por el virus Zika (ZIKV), del género Flavivirus.
La enfermedad se desarrolla entre 3 y 12 días después de la picadura del vector. Una de cada cuatro personas puede no desarrollar síntomas, pero en quienes se ven afectados, la enfermedad es usualmente leve, con síntomas que pueden durar entre 2 y 7 días. Ha sido también descrita una transmisión perinatal y posiblemente sexual. La transmisión asociada a transfusiones es posible, ya que el ZIKV ha sido identificado en donantes de sangre asintomáticos durante la aparición de un brote de la enfermedad.
La apariencia clínica es muchas veces similar a la del dengue. Los hallazgos clínicos son fiebre de inicio agudo, con erupción principalmente máculo-papular, artralgias o conjuntivitis no purulenta. Otros síntomas incluyen malestar general, mialgias, cefalea, dolor retro-orbitario y vómitos. Los síntomas usualmente duran de varios días a una semana. La enfermedad grave no es común y son raros los casos fatales (existe un caso comunicado de síndrome de Guillain-Barré en un paciente con probable infección por ZIKV).
Durante la primera semana la fiebre ZIKA puede ser diagnosticada realizando RT-PCR en suero. Los anticuerpos neutralizantes e IgM virus-específicos típicamente se desarrollan hacia el final de la primera semana; existe reacción cruzada con flavivirus relacionados y puede ser difícil discernir entre ellos. Puede ser realizado el análisis de neutralización reducción de placa para medir anticuerpos neutralizantes específicos de virus y así discriminar entre anticuerpos con reacción cruzada en infecciones primarias por flavivirus.
El tratamiento incluye reposo, líquidos y analgésicos-antipiréticos. Sin embargo, debe ser evitada la aspirina y otros AINE hasta que se pueda descartar dengue para reducir el riesgo de hemorragia.
Conclusión
Las arbovirosis son un grupo de enfermedades que solo pueden ser eliminadas con la participación de toda la sociedad y los diferentes gobiernos, con un control sanitario estricto y evitando el silencio epidemiológico2,3,25.
Conflicto de intereses
Los autores declaran que no existen conflictos de intereses en relación con esta investigación.
Bibliografía
- Sarti E, Cox H, Besada-Lombana S, Tapia-Maruri L. Dengue awareness in Latin American populations: A questionnaire study. Infect Dis Ther. 2015; 4: 199-211.
- Ochoa OMR, Casanova MMC, Díaz DMA. Análisis sobre el dengue, su agente transmisor y estrategias de prevención y control. AMC. 2015; 19: 189-202.
- Betancourt-Cravioto M, Kuri-Morales P, González-Roldán JF, Tapia-Conyer R. Mexican Dengue Expert Group. Introducing a dengue vaccine to Mexico: development of a system for evidence-based public policy recommendations. PLoS Negl Trop Dis. 2014; 8: e3009.
- Mourão MPG, Bastos MS, Figueiredo RMP, Gimaque JBL, Alves VCR, Saraiva MGG, et al. Arboviral diseases in the Western Brazilian Amazon: a perspective and analysis from a tertiary health & research center in Manaus, State of Amazonas. Rev Soc Bras Med Trop. 2015; 48(suppl 1): 20-6.
- Conde M, Orjuela LI., Castellanos CA, Herrera-Varela M, Licastro S, Quiñones ML. Evaluación de la sensibilidad a insecticidas en poblaciones de Aedes aegypti (Diptera: Culicidae) del departamento de Caldas, Colombia, en 2007 y 2011. Biomédica. 2015; 35: 43-52.
- Manore CA, Hickmann KS, Xu S, Wearing HJ, Hyman JM. Comparing dengue and chikungunya emergence and endemic transmission in A. aegypti and A. albopictus. J Theor Biol. 2014; 356: 174-91.
- Bouzid M, Colón-González FJ, Lung T, Lake IR, Hunter PR. Climate change and the emergence of vector-borne diseases in Europe: case study of dengue fever. BMC Public Health. 2014; 14: 781.
- Torres-Galicia I, Cortés-Poza D, Becker I. Dengue en México: incremento en la población juvenil durante la última década. Bol Med Hosp Infant Mex. 2014; 71: 196-201.
- Che-Mendoza A, Guillermo-May G, Herrera-Bojórquez J, Barrera-Pérez M, Dzul-Manzanilla F, Gutiérrez-Castro C, et al. Long-lasting insecticide-treated house screens and targeted treatment of productive breeding-sites for dengue vector control in Acapulco, México. Trans R Soc Trop Med Hyg. 2015; 109: 106-15.
- Cruz LC, Serra OP, Leal-Santos FA, Ribeiro AL, Slhessarenko RD, Santos MA. Natural transovarial transmission of dengue virus 4 in Aedes aegypti from Cuiabá, State of Mato Grosso, Brazil. Rev Soc Bras Med Trop. 2015; 48: 18-25.
- Castellanos J, Bello J, Velandia-Romero M. Manifestaciones neurológicas durante la infección por el virus del dengue. Infectio. 2014; 18: 167-76.
- Dayan G, Arredondo JL, Carrasquilla G, Deseda CC, Dietze R, Luz K, et al. Prospective cohort study with active surveillance for fever in four dengue endemic countries in Latin America. Am J Trop Med Hyg. 2015; 93: 18-23.
- Araujo RV, Albertini MR, Costa-da-Silva AL, Suesdek L, Franceschi NC, Bastos NM, et al. São Paulo urban heat islands have a higher incidence of dengue than other urban areas. Braz J Infect Dis. 2015; 19: 146-55.
- Palma-Ocampo HK, Flores-Alonso JC, Vallejo-Ruiz V, Reyes-Leyva J, Flores-Mendoza L, Herrera-Camacho I, et al. Interferon lambda inhibits dengue virus replication in epithelial cells. Virol J. 2015; 12: 150.
- Chuc S, Hurtado-Díaz M, Schilmann A, Riojas-Rodríguez H, Rangel H, González-Fernández MI. Condiciones locales de vulnerabilidad asociadas con dengue en dos comunidades de Morelos. Salud pública Méx. 2013; 55: 170-8.
- Bottazzi ME, Dumonteil E, Valenzuela JG, Betancourt-Cravioto M, Tapia-Conyer R, Hotez Peter J. Bridging the innovation gap for neglected tropical diseases in México: capacity building for the development of a new generation of antipoverty vaccines. Bol Med Hosp Infant Mex. 2011; 68: 150-8.
- Morato DG, Barreto FR, Braga JU, Natividade MS, Costa MdCN, Morato V, et al. The spatiotemporal trajectory of a dengue epidemic in a medium-sized city. Mem Inst Osw Cruz. 2015; 110: 528-33.
- Quintero J, Brochero H, Manrique-Saide P, Barrera-Pérez M, Basso C, Romero S, et al. Ecological, biological and social dimensions of dengue vector breeding in five urban settings of Latin America: a multi-country study. BMC Infect Dis. 2014; 14: 38.
- Villegas-Trejo A, Che-Mendoza A, González-Fernández M, Guillermo-May G, González-Bejarano H, Dzul-Manzanilla F, et al. Control enfocado de Aedes aegypti en localidades de alto riesgo de transmisión de dengue en Morelos, México. Salud Pública Méx. 2011; 53: 141-51.
- Vilcarromero S, Casanova W, Ampuero JS, Ramal-Asayag C, Siles CDG. Lecciones aprendidas en el control de Aedes aegypti para afrontar el dengue y la emergencia de chikungunya en Iquitos, Perú. Rev Peru Med Exp Salud Publ. 2015; 32: 172-8.
- Osorio L, Uribe M, Ardila GI, Orejuela Y, Velasco M, Bonelo A, et al. The use of rapid dengue diagnostic tests in a routine clinical setting in a dengue-endemic area of Colombia. Mem Inst Osw Cruz. 2015; 110: 510-6.
- Vázquez-Pichardo M, Rosales-Jiménez C, Núñez-León A, Rivera-Osorio P, Cruz-Hernández S, Ruiz-López A, et al. Serotipos de dengue en México durante 2009 y 2010. Bol Med Hosp Infant Mex. 2011; 68: 103-10.
- Pancetti FG, Honório NA, Urbinatti PR, Lima-Camara TN. Twenty-eight years of Aedes albopictus in Brazil: a rationale to maintain active entomological and epidemiological surveillance. Rev Soc Bras Med Trop. 2015; 48: 87-9.
- Hadinegoro SR, Arredondo-García JL, Capeding MR, Deseda C, Chotpitayasunondh T, Dietze R, et al; CYD-TDV Dengue Vaccine Working Group. Efficacy and long-term safety of a Dengue vaccine in regions of endemic disease. N Engl J Med. 2015; 373: 1195-206.
- Valencia-Mendoza A, Danese-dlSantos LG, Sosa-Rubí SG, Aracena-Genao B. Costo-efectividad de prácticas en salud pública: revisión bibliográfica de las intervenciones de la Iniciativa Mesoamericana de Salud. Salud Pública Méx 2011; 53(suppl 3): s375-s385.