Clínica Cotidiana
Información del artículo
Historia del artículo:
Recibido el 24 de octubre de 2017
Aceptado el 16 de mayo de 2018
On-line el 27 de septiembre de 2018
Palabras clave:
Enfermedad pulmonar intersticial
Nitrofurantoína
Mesalazina
Efectos secundarios
*Autor para correspondencia
Correo electrónico:
miriamgr75@hotmail.com
(M. García Revuelta)
Keywords:
Interstitial lung disease
Nitrofurantoin
Mesalazine
Side effects
Míriam García Revuelta*, María Antonia del Valle Martín, María Varela Patiño
Centro de Salud Arturo Eyríes. Valladolid.
Resumen
Las enfermedades intersticiales difusas del pulmón (EPID)1 constituyen un grupo muy heterogéneo de afecciones con manifestaciones clínicas, radiológicas y funcionales comunes, en las cuales las principales alteraciones anatomo-patológicas afectan a estructuras alveolo-intersticiales.
En España la incidencia estimada de EPID es de 7,6 casos/100.000 habitantes; la más frecuente es la fibrosis pulmonar idiopática (FPI), con una incidencia de 1,6 casos/100.000 habitantes.
Entre los agentes causales relativamente frecuentes que pueden provocar EPID se encuentra una amplia lista de fármacos; la mesalazina y la nitrofurantoína forman parte de esta. Por este motivo se presenta un caso con clínica respiratoria por consumo de estos fármacos.
© 2018 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Drug induced interstitial lung disease
Abstract
The interstitial lung diseases (ILD), are a heterogeneous group of disorders that are classified together because of similar clinical, radiographic and functionals manifestations where in the main anatomo-pathological alterations affect alveolar-interstitial structures.
The incidence of ILD in Spain is approximately 7.6 cases per 100000 inhabitants, being the most frequent disease the Idiopathic pulmonary fibrosis with an incidence 1.6 cases per 100000 inhabitants.
The most common identifiable causes of ILD are an extensive list of drugs such as mesalazine and nitrofurantoin wich are part of it. For this reason a clinical case is presented in wich the patient had pulmonary symptoms because of taking this drugs.
© 2018 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Mujer de 83 años de edad, con antecedentes personales de cardiopatía tratada con antihipertensivos, colitis colágena en tratamiento con mesalazina (3 g/día durante el brote agudo) e infecciones del tracto urinario (ITU) de repetición en tratamiento profiláctico con nitrofurantoína (50 mg/día) desde hace un año.
Acude a consulta por presentar tos seca intermitente y disnea de moderados esfuerzos desde hace un mes. No mejora con la azitromicina pautada en Urgencias.
En la exploración física la paciente se encuentra afebril, con saturación de oxígeno 88 %; auscultación cardiaca: soplo sistólico en el foco aórtico; auscultación pulmonar: crepitantes bibasales; resto de la exploración normal.
En la radiografía de tórax se observa la presencia de patrón intersticial bilateral (Fig. 1).
El diagnóstico diferencial2 debe realizarse con patologías que pueden cursar con manifestaciones clínicas y radiológicas pulmonares similares, como insuficiencia cardiaca, bronquiectasias, neumonía lipoidea, tuberculosis miliar, enfermedad pulmonar obstructiva crónica, asma, linfangitis carcinomatosa, carcinoma broncoalveolar, síndrome linfoproliferativo, hemorragias pulmonares difusas, tuberculosis miliar y enfermedad miliar por el bacilo de Calmette-Guérin.
Se remite a la paciente a Urgencias para la confirmación del diagnóstico.
Durante su ingreso en el hospital se le realizan las siguientes pruebas complementarias:
Analítica: sistemático de sangre, bioquímica con anticuerpos antinucleares, serologías de neumonías atípicas normales.
Antígenos en orina para Legionella y Neumococo: negativos.
Exudado de virus respiratorios y gripe A: negativos.
Radiografía de tórax: pérdida de volumen en el hemitórax izquierdo; imágenes parcheadas de aumento de densidad en ambos hemitórax.
Espirometría: patrón restrictivo.
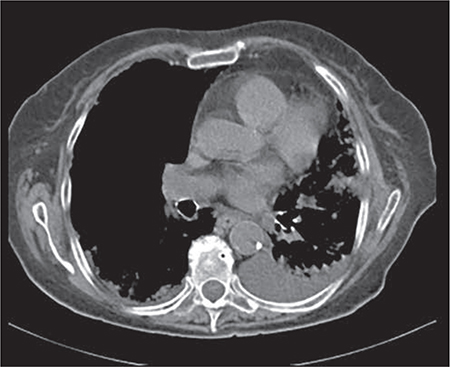
Tomografía axial computarizada (TAC): imágenes de condensación parenquimatosa con broncograma aéreo unido a áreas de condensación en vidrio deslustrado, de distribución parcheada en ambos hemitórax, más acusado en el lado izquierdo; derrame pleural izquierdo (Fig. 2).
Broncoscopia: imposibilidad de realización de lavado broncoalveolar (BAL) por desaturación a 83 %.
Microbiología de broncoaspirado (BA): flora bacteriana normal. Citología de BAS: negativo para células tumorales.
Baciloscopia: negativa.
Cultivo de micobacterias: negativo.
Se pauta tratamiento antibiótico (piperacilina-tazobactam) y corticoides. La evolución es favorable. Se decide la retirada de nitrofurantoína dada la sospecha de EPID. Se realiza valoración por Digestivo para descartar patología intersticial secundaria a mesalazina y se suspende esta a pesar de que se considera un efecto adverso muy raro.
Figura 1 –
Figura 2 –
Al alta la paciente presenta mejoría clínica.
A los dos meses del alta y de la retirada de ambos fármacos la paciente es revisada en consulta, donde se observa una mejoría radiológica (disminución del patrón intersticial y persistencia de mínimas imágenes en la base derecha) (Fig. 3) y desaparición por completo de la clínica respiratoria. La espirometría presenta valores dentro de la normalidad.
En este caso no se puede demostrar cuál fue el fármaco responsable de la clínica de la paciente, ya que ambos pueden producir EPID como efecto adverso infrecuente; al suspender los dos en el mismo intervalo de tiempo no se puede conocer la relación causal con uno en concreto.
Figura 3 – Imagen de broncoscopia flexible: masa que ocluye en su totalidad la entrada del bronquio subsegmentario medial.
Comentarios
Uno de los posibles agentes causales de EPID es la toma crónica de nitrofurantoína como prevención de las ITU de repetición.
La incidencia de toxicidad pulmonar por este medicamente es de 1 %3. Se da con más frecuencia en mujeres debido a la mayor exposición a nitrofurantoína por ITU de repetición4. La media de edad es de 60-70 años.
La forma de presentación suele ser aguda5. Aparece al cabo de pocas horas de la primera exposición al fármaco hasta una semana después. Cursa con tos, disnea, fiebre, dolor torácico y artralgias. No parece estar relacionada con la dosis6.
La forma crónica es más difícil de reconocer6 debido al inicio insidioso de los síntomas y al largo intervalo desde el inicio del tratamiento hasta la presentación de la reacción adversa pulmonar. Puede desarrollarse desde 1 mes hasta varios años después de haberse iniciado el tratamiento. Suele aparecer tos insidiosa, disnea progresiva (como el caso de nuestra paciente), pero también puede asociarse a dolor torácico, pérdida ponderal y mialgias. El mecanismo de toxicidad es dosis-dependiente7.
Otro agente causal de EPID relacionado con nuestro caso puede ser la mesalazina, tratamiento utilizado para la enfermedad inflamatoria intestinal (EII).
Las alteraciones pulmonares por mesalazina están recogidas en la ficha técnica como reacciones “muy raras” (1/10.000 pacientes)8. La revisión publicada por Sossai et al9 afirma que la media de edad de presentación es de 46 años (rango: 15-72 años) y que las mujeres lo padecían con más frecuencia que los hombres. La aparición de los síntomas10 puede seguir una secuencia temporal tras la administración del fármaco (2-10 días tras la toma del mismo), pero también existen casos en los que aparecen tres meses o incluso años después del tratamiento con mesalazina. Los pacientes pueden estar desde asintomáticos con algún hallazgo radiográfico hasta presentar fiebre, tos, disnea o astenia.
Con ambos fármacos la consecuencia en la función pulmonar puede ser un patrón restrictivo con una disminución de la difusión del dióxido de carbono.
Los hallazgos en la radiografía de tórax11 son inespecíficos: patrón alveolar o intersticial con derrame pleural.
Lo que verdaderamente ayuda al diagnóstico es la TAC, en la que podemos visualizar un patrón en vidrio deslustrado, áreas de consolidación o densidades reticulares.
En la broncoscopia y el BAL puede aparecer linfocitosis y eosinofilia.
Otros fármacos12 no relacionados con nuestro caso que provocan EPID son antibióticos como etambutol o minociclina, metotrexato, antiinflamatorios no esteroideos, antiarrítmicos como amiodarona o procainamida, antineoplásicos como azatioprina, estatinas; también se ha implicado a la infección por el bacilo de Calmette-Guérin (BCG).
Lo que confirma por completo el diagnóstico es la relación temporal entre la toma del fármaco y la aparición de la clínica respiratoria; sin embargo, muchas veces esta demostración no se puede llevar a cabo debido a las reacciones adversas que aparecen tras años de tratamiento, como ya se ha comentado.
La base del tratamiento es sin duda la retirada del fármaco y la observación de la evolución de la paciente, en la que se produce la consecuente mejoría clínica y radiológica.
El uso de los corticoides en el tratamiento de la toxicidad pulmonar inducida tanto por nitrofurantoína como mesalazina es controvertido6. Algunos autores recomiendan el tratamiento con corticoides (1 mg/kg), ya que facilitan una rápida recuperación.
En resumen, es importante hacer un buen control cuando se administra este tipo de fármacos, sobre todo la nitrofurantoína5. Cada vez están apareciendo más alertas debido a los efectos adversos, sobre todo pulmonares. La última comunicación de la Agencia Española del Medicamento13 recomienda utilizar nitrofurantoína como tratamiento curativo de ITU con una duración máxima de 7 días, no como tratamiento profiláctico.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Banderas ME, Sánchez B. Enfermedades pulmonares intersticiales difusas. En: Suárez D, Vargas JC, Salas J, et al (eds). Manual de diagnóstico y terapéutica médica. Hospital Universitario 12 de Octubre. 8ª ed. Madrid; 2016. p. 541-9.
- Xaubet A, Ancochea J, Blanquer R, Montero C, Morell F, Rodríguez E, et al. Diagnóstico y tratamiento de las enfermedades pulmonares intersticiales difusas. Arch Bronconeumol 2003; 39: 580-600.
- Zeeuw J, Gillissen A. Nitrofurantoin-induced pulmonary injury. [monografía en internet]. En: Uptodate. Flaherty KR, Hollingsworth H [actualizado Febrero 2017; acceso: 28 de febrero de 2017]. Disponible en: https://uptodate.publicaciones.saludcastillayleon.es/contents/nitrofurantoin-induced-pulmonary
- Núñez MA, Fernández A, Velasco J, Gómez JJ, García C, Hernández JL. Nitrofurantoína y enfermedad pulmonar intersticial de rápida resolución. Arch Bronconeumol. 2009; 45: 352-5.
- Kanji Z, Su VC, Mainra R. Nitrofurantoin-induced pulmonary reaction involving respiratory symptoms: Case report. Can J Hosp Pharm. 2011; 64: 362-5.
- Valiño P, Fernández MM, Santamaría B. Toxicidad pulmonar crónica por nitrofurantoína. Pneuma. 2010; 6: 76-8.
- Machado JM, Ortega A, Flores J. Toxicidad pulmonar crónica por nitrofurantoína. Med Gen y Fam. 2015; 4: 85-8.
- Neumonitis intersticial por mesalazina en paciente con colitis ulcerosa. Farm Hospital. 2016; 40: 55-7.
- Sossai P, Cappellato MG, Stefani S. Can a drug-induced pulmonary hypersensitivity reaction be dose-dependent? A case with mesalamin. Mt Sinai J Med. 2001; 68: 389-95.
- Alskaf E, Aljoudeh A, Edenborough F. Mesalazine-induced lung fibrosis. BMJ Case Rep. 2013; 2013. doi: 10.1136/bcr-2013-008724.
- Abraham A, Karakurum A. Acute respiratory failure secondary to mesalamine-induced interstitial pneumonitis. BMJ Case Rep. 2013; 2013. doi: 10.1136/bcr-2013-009834.
- King T. Approach to the adult with interstitial lung desease: clinical evaluation. [monografía en internet]. En: Uptodate. Flaherty KR, Hollingsworth H. [actualizado Mayo 2018; acceso: 06-06-2018]. Disponible en: https://uptodate.publicaciones.saludcastillayleon.es/contents/approach-to-the-adult-with-interstitial-lung-disease-clinical-evaluation
- Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Nitrofurantoína: nuevas restricciones de uso. Disponible en: https://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/seguridad/2016/docs/NI-MUH_FV_16-nitrofurantoina.pdf