Artículo de Revisión
Información del artículo
Historia del artículo:
Recibido el 23 de octubre de 2020
Aceptado el 19 de enero de 2021
On-line el 21 de julio de 2021
Palabras clave:
Dolor neuropático
Farmacoterapia
Atención primaria
Recomendaciones
Terapias emergentes
*Autor para correspondencia
Correo electrónico:
a.alcantara.montero@hotmail.com
(A. Alcántara Montero).
Keywords:
Neuropathic pain
Pharmacotherapy
Primary care
Recommendations
Emerging therapies
Antonio Alcántara Monteroa,*, Sandra Raquel Pacheco de Vasconcelosb
aCentro de Salud Manuel Encinas. Consultorio de Malpartida de Cáceres, Cáceres. bComplejo Hospitalario Universitario de Cáceres. Hospital Universitario, Cáceres.
Resumen
El dolor neuropático es el causado por una lesión o enfermedad del sistema nervioso somatosensorial y representa un problema sociosanitario de gran envergadura, que afecta a un grupo importante de la población. Es el resultado de múltiples causas y puede presentarse como una gran variedad de síndromes. Esta situación nos ofrece la oportunidad de actualizar su conocimiento con el fin de tomar las mejores decisiones posibles en su abordaje clínico diario.
En esta segunda parte revisamos el tratamiento y los criterios de derivación a Unidades de Tratamiento del Dolor desde atención primaria. Los objetivos que se pretenden conseguir al tratar el dolor neuropático son la reducción del dolor y una mejora funcional y de la calidad de vida. El tratamiento es multimodal y pueden proponerse medidas no farmacológicas y farmacológicas. Futuras perspectivas engloban el desarrollo de nuevos fármacos y un abordaje terapéutico con un enfoque más personalizado, que es posible gracias a los recientes avances en la evaluación y comprensión del dolor neuropático.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Update in the diagnostic and therapeutic approach of neuropathic pain from primary care (II)
Abstract
Neuropathic pain is pain caused by a lesion or disease of the somatosensory nervous system, and represents a large social and health problem, which concerns an important group of the population. It is the result of multiple etiologies and can be presented as a great variety of syndromes. This situation offers us the opportunity to update your knowledge in order to make the best possible decisions in your daily clinical management.
In this second part we review the treatment and referral criteria to Pain Treatment Units from primary care. The aims to be achieved when treating neuropathic pain are the reduction of pain and an improvement in function and quality of life. Treatment is multimodal and non-pharmacological and pharmacological measures can be proposed. Future perspectives include the development of new drugs and a therapeutic approach with a more personalized focus, made possible by recent advances in the assessment and understanding of neuropathic pain.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Tratamiento
Los objetivos que se pretenden conseguir al tratar el dolor neuropático son la reducción del dolor y una mejora funcional y de la calidad de vida. El tratamiento es multimodal y pueden proponerse medidas no farmacológicas y farmacológicas. Para clasificar la calidad de la evidencia y fuerza de las recomendaciones hemos empleado la clasificación SORT (Strength Of Recommendation Taxonomy), empleada por diversas revistas médicas del ámbito americano de la Atención Primaria (American Family Physician, Journal of Family Practice, Journal of American Board Family Practice).
Tratamiento no farmacológico
Las medidas no farmacológicas incluyen la información y educación al paciente, la terapia física y las técnicas psicológicas1.
Información y educación
Es muy importante la relación médico-paciente, ofrecer información adecuada y comprensible, así como contemplar objetivos realistas. Una reducción del 30 % del dolor es relevante y puede considerarse una respuesta parcial. La participación del paciente en la toma de decisiones es esencial. Por otro lado, al paciente hay que educarle en la adherencia al tratamiento; debe saber que los fármacos que habitualmente se emplean en el dolor neuropático pueden tener efectos adversos (náuseas y vómitos, somnolencia, mareos o inestabilidad).
Medidas psicológicas
La terapia cognitiva y el soporte psicoterapéutico han demostrado ser efectivos en el tratamiento del dolor neuropático periférico. El papel de la terapia cognitivo-conductual (TCC) es ayudar a los pacientes a reconocer los factores emocionales y psicológicos que influyen en la percepción del dolor y las conductas asociadas (grado de recomendación A)2. El catastrofismo es un predictor de mal pronóstico y de mala respuesta al tratamiento farmacológico. Los pacientes tienen el convencimiento en muchas ocasiones de que la actividad provocará más dolor y aumentará la discapacidad. La TCC pretende modificar pensamientos y emociones a través de técnicas de afrontamiento positivo.
Terapia física
El dolor neuropático puede ser causa de disminución de la actividad física y la funcionalidad. La terapia física y el ejercicio son medidas que contribuyen a evitar la pérdida de la función debido a comportamientos de evitación. Un tratamiento efectivo debe centrarse tanto en la mejoría de los síntomas como en la restauración funcional y la movilización. La evidencia disponible sugiere que la actividad física y el ejercicio constituyen una intervención con pocos efectos adversos y que pueden mejorar la gravedad del dolor y la función física, con la consiguiente calidad de vida. Sin embargo, se requiere más investigación y debe centrarse en aumentar el número de participantes, incluidos los participantes con un espectro más amplio de gravedad del dolor, y alargar tanto la intervención en sí misma como el periodo de seguimiento (grado de recomendación B)3.
No hay pruebas suficientes para apoyar o refutar el uso de la acupuntura en el dolor neuropático en general, o para cualquier afección específica del dolor neuropático en comparación con la acupuntura simulada u otras terapias activas. Existen estudios que están en curso y otros en espera de clasificación debido a la duración incierta del tratamiento, y los resultados de estos estudios pueden influir en los resultados de revisiones ya publicadas (grado de recomendación B)4.
La estimulación nerviosa eléctrica transcutánea (TENS) es una modalidad de tratamiento no invasiva, inocua y de aplicación sencilla. En una revisión Cochrane se informó sobre la comparación entre la TENS y la TENS inactiva. La calidad de la evidencia fue muy baja, lo que significa que no fue posible establecer con seguridad si la TENS es efectiva para el control del dolor en los pacientes con dolor neuropático. La calidad muy baja de la evidencia significa que existe una confianza muy limitada en el cálculo del efecto informado; es probable que el efecto verdadero sea significativamente diferente (grado de recomendación B)5.
Tratamiento farmacológico
Numerosas recomendaciones terapéuticas para el dolor neuropático se han propuesto en la última década6-10. El grupo de interés especial en dolor neuropático de la Asociación Internacional para el Estudio del Dolor (NeuPSIG, por sus siglas en inglés, Special Interest Group on Neuropathic Pain) publicó en 2015 una guía para el tratamiento farmacológico del dolor neuropático basada en una revisión sistemática y metaanálisis de ensayos publicados y no publicados11; se excluyó la neuralgia del trigémino, para la cual han sido publicadas guías específicas12. Dichas recomendaciones incluyeron estudios aleatorizados, controlados con placebo, doble ciego, con fármacos utilizados por vía oral o tópica en dosis repetidas, excepto para agentes con eficacia a largo plazo después de una única aplicación (por ejemplo, parches de capsaicina al 8 %).
Fármacos recomendados en primera línea (grado de recomendación A)11,13
Se ha confirmado la eficacia de los antidepresivos tricíclicos (ADT), especialmente amitriptilina, y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), en particular duloxetina, en varias condiciones de dolor neuropático y se recomiendan en primera línea (Tabla 1)13. Los ADT y los IRSN actúan inhibiendo la recaptación de serotonina y noradrenalina, con lo que aumentan así el control inhibitorio. Los ADT también actúan sobre los canales de sodio, los receptores beta2-adrenérgicos, los receptores opioides y tienen efecto antagonista sobre el receptor N-metil-D-aspartato (NMDA), así como efectos anticolinérgicos y antihistamínicos13.
Los efectos secundarios incluyen somnolencia, mareos, sequedad de boca e hipotensión ortostática. Los ADT pueden causar una prolongación del intervalo QT, por lo que se recomienda realizar un ECG antes de iniciar el tratamiento, especialmente en los ancianos13. Aunque la amitriptilina ha sido la más estudiada y es la única que tiene indicación según la EMA (Agencia Europea de Medicamentos) y la AEMPS (Agencia Española de Medicamentos y Productos Sanitarios), todos los ADT tienen una eficacia similar en el dolor neuropático. Las aminas secundarias (nortriptilina, desipramina) tienen menos efectos secundarios sedantes. Las aminas terciarias (amitriptilina, imipramina, clomipramina) no se recomiendan en dosis superiores a 75 mg/día en pacientes mayores de 65 años de edad debido a sus efectos sedantes, anticolinérgicos y el consiguiente riesgo de caídas13.
La eficacia de la pregabalina y la gabapentina está bien establecida para el tratamiento del dolor neuropático periférico; la pregabalina es el único fármaco con indicación en dolor neuropático central. Sus efectos analgésicos se relacionan principalmente con una disminución de la sensibilización central mediante la unión a la subunidad α2-δ de los canales de calcio voltaje-dependientes. Mareos y somnolencia son los efectos secundarios más frecuentes y las dosis deben ajustarse en pacientes con insuficiencia renal13.
Fármacos recomendados en segunda línea (grado de recomendación B)11,13
Los tratamientos de segunda línea incluyen agentes tópicos para el dolor neuropático periférico (Tabla 1)11. Los apósitos de lidocaína al 5 % producen un efecto analgésico local al inhibir los canales de sodio voltaje-dependientes de los nervios dañados por la lesión. Estos canales ectópicos son estabilizados por la lidocaína; de este modo se produce analgesia sin efecto anestésico local asociado13. Los apósitos contienen 700 mg de principio activo por apósito. El área dolorosa debe cubrirse con el apósito una vez al día durante un intervalo de tiempo que, como máximo, debe ser de 12 horas. Los apósitos pueden cortarse en tamaños más pequeños antes de retirar la lámina de liberación. No deben utilizarse más de tres apósitos de 14 x 10 cm al mismo tiempo (o sobre una superficie total mayor de 420 cm2). Presentan una excelente tolerabilidad y buena eficacia. Debido a la escasa absorción, su tolerabilidad sistémica es buena, aunque se puede producir algún efecto irritativo local; el potencial de interacciones es mínimo. Los apósitos deben aplicarse sobre zonas de piel intacta, seca, no irritada y sin pelos. No debe aplicarse sobre áreas de piel inflamada o lesionada, heridas, dermatitis atópica o mucosas. Están indicados en el alivio sintomático del dolor neuropático asociado a infección previa por herpes zóster (neuralgia postherpética), pero se ha demostrado su utilidad fuera de indicación en otros tipos de dolor neuropático localizado (DNL), como la polineuropatía diabética, la polineuropatía sensorial idiopática y el dolor postquirúrgico y postraumático, pues disminuye el tamaño de la zona de alodinia asociada a este tipo de dolor13.
La capsaicina es un agonista selectivo del receptor TRPV1 (receptor de potencial transitorio vaniloide tipo 1). El estímulo inicial de estos receptores cutáneos produce dolor y eritema, causados por la liberación de neuropéptidos vasoactivos, sustancia P (SP), para posteriormente producirse una depleción de SP y desensibilización de los nociceptores cutáneos, que pierden parte de su sensibilidad a diversos estímulos. El parche de capsaicina al 8 % (179 mg capsaicina por parche) se aplica sobre la piel durante 30 a 60 minutos, dependiendo de la localización del dolor. Se podrá administrar un anestésico tópico en la zona de tratamiento o un analgésico oral al paciente antes de aplicar este parche, para reducir las posibles molestias propias de la aplicación. El anestésico tópico deberá cubrir toda la zona de tratamiento con el parche de capsaicina más un borde de 1 a 2 cm. En los ensayos clínicos los pacientes recibieron pretratamiento con lidocaína tópica (4 %), lidocaína (2,5 %) más prilocaína (2,5 %) o 50 mg de tramadol. Hasta cuatro parches pueden ser aplicados en un mismo momento y el tratamiento se puede repetir cada 3 meses tantas veces como sea necesario. En la práctica clínica proporciona un alivio del dolor rápido y sostenido en pacientes con diversas condiciones de neuropático periférico, y reduce significativamente la prescripción de medicación analgésica concomitante. Los principales efectos adversos son transitorios: reacciones locales en el lugar de aplicación, principalmente dolor y eritema13.
Algunos autores señalan que los tratamientos tópicos deben ser considerados como primera línea en el abordaje del DNL y en población vulnerable (ancianos, polimedicados, con comorbilidades…), debido a que la relación beneficio/riesgo es mucho mejor que la de los agentes sistémicos. La aplicación tópica se presenta como un tratamiento local, con una menor dosis total sistémica y evita el primer paso hepático, lo que reduce el riesgo de efectos adversos e interacciones farmacológicas13 (Fig. 1).
Figura 1 – Algoritmo de tratamiento del dolor neuropático periférico en Atención Primaria (adaptada de ref. 13).
Se ha demostrado que el tramadol, un opioide débil que inhibe la recaptación de serotonina y noradrenalina, es beneficioso principalmente en dolor neuropático periférico (Tabla 1). Se recomienda este medicamento como segunda línea, principalmente debido al riesgo potencial de abuso (aunque menos que con opioides potentes) y riesgo de confusión y somnolencia, particularmente en los ancianos. Debe ser utilizado con precaución cuando se asocia con antidepresivos13.
Fármacos recomendados en tercera línea (grado de recomendación B)11,13
Los opioides potentes (particularmente oxicodona, morfina y tapentadol) son moderadamente eficaces en el tratamiento del dolor neuropático periférico. Además, existe preocupación por el aumento de la prescripción, sobredosis, mal uso y morbilidad asociada a opioides13. Por tanto, estos medicamentos se recomiendan como de tercera línea de tratamiento (Tabla 1)13.
Se ha demostrado la eficacia de la toxina botulínica tipo A (BTX-A), una potente neurotoxina comúnmente utilizada para el tratamiento de la hiperactividad muscular focal, hasta tres meses después de su administración en un conjunto de inyecciones únicas, posiblemente a través de un efecto central (Tabla 1). La BTX-A es administrada en el ámbito de atención hospitalaria por vía subcutánea en dosis de 50 a 200 UI repartidas sobre el área del dolor. La inyección es dolorosa, por lo que pueden usarse anestésicos locales e inhalación de óxido nitroso al 50 % y oxígeno antes y durante todo el tratamiento para minimizar el dolor. Además del dolor sobre la zona de aplicación, el tratamiento generalmente se considera seguro, aunque hay experiencia limitada de estudios a largo plazo. La BTX-A debe ser utilizada por especialistas como última opción en casos refractarios de dolor neuropático periférico y en zonas limitadas de dolor13.
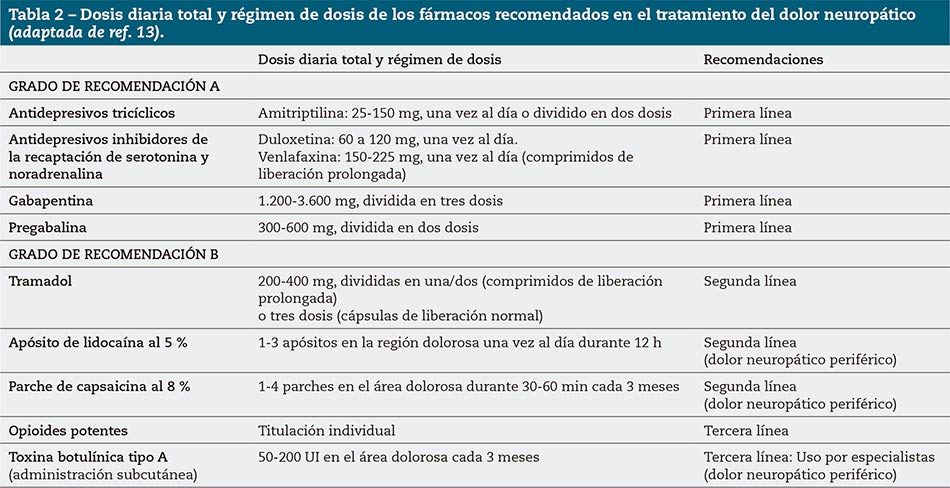
En la tabla 2 se recogen la dosis diaria total y el régimen de dosis de los fármacos recomendados en el tratamiento del dolor neuropático13.
Fármacos con resultados inconsistentes o falta de eficacia en dolor neuropático (grado de recomendación C)11,13
Los estudios con otros antiepilépticos distintos de los ligandos α2-δ de los canales de calcio (por ejemplo, topiramato, oxcarbazepina, carbamazepina, acetato de eslicarbazepina, valproato, lacosamida, levetiracetam) han reportado resultados negativos, débiles o inconsistentes, aunque medicamentos como la oxcarbazepina son probablemente efectivos en algunos subgrupos de pacientes.
Se ha reportado una eficacia variable de los cannabinoides oromucosos (2,7 mg delta-9-tetrahidro-cannabinol/2,5 mg cannabidiol), particularmente en el dolor asociado a la esclerosis múltiple; sin embargo, varios ensayos clínicos no publicados obtuvieron resultados negativos en los objetivos primarios.
Los resultados para los inhibidores selectivos de la recaptación de serotonina (ISRS), antagonistas de los receptores NMDA, mexiletina y clonidina tópica han sido generalmente inconsistentes o negativos13.
Nuevos fármacos en desarrollo clínico para el dolor neuropático
Se están desarrollando actualmente más de 100 moléculas que actúan en dianas específicas de potencial interés para el dolor neuropático. Entre ellas están incluidas antagonistas específicos de las isoformas de los canales de sodio, antagonistas de receptores vaniloides, agonistas de los canales de potasio, antagonistas de los receptores metabotrópicos del glutamato/NMDA o nuevos moduladores de los receptores NMDA, nuevos agonistas de receptores opioides, antagonistas del receptor H3 de la histamina, moduladores serotoninérgicos, agonistas nicotínicos, agonistas adrenérgicos, inhibidores de la óxido nítrico sintasa, antagonistas de los receptores de la orexina, antagonistas de los receptores de la angiotensina tipo II, agonistas del receptor I2 de imidazolinas, inhibidores de la apoptosis, agonistas del receptor cannabinoide CB2, antagonistas selectivos del receptor sigma-1, inhibidores de la amida hidrolasa de ácidos grasos, moléculas anti factor de crecimiento nervioso, terapia genética…14.
Criterios de derivación
Los criterios generales de derivación de pacientes con dolor neuropático desde atención primaria a Unidades de Tratamiento del Dolor (UTD) incluyen15:
- Dolor crónico diagnosticado no controlado que el médico de atención primaria estime oportuno.
- Necesidad de una orientación por las UTD en el inicio de una terapia antiálgica a seguir por el médico de atención primaria.
- Cuando no se consiga una mejora funcional y de la calidad de vida.
- Si al cabo de tres meses de tratamiento y seguimiento adecuado con un plan integral de tratamiento la intensidad del dolor o la funcionalidad no han alcanzado los objetivos, debe considerarse como un cuadro de dolor crónico de difícil control, tributario de interconsulta (telefónica/presencial) a la UTD.
- Apoyo por la UTD cuando se trate de pacientes complejos o polimedicados en los que se presenten o puedan presentar efectos adversos intolerables con la medicación o interacciones importantes.
- Pacientes con sobreuso de analgésicos por toxicomanía.
- Alto consumo de rescates.
- El paciente debe ser atendido en la UTD en estrecha coordinación con su equipo de atención primaria. El plan de acción compartida se activará por acuerdo entre los responsables del paciente cuando este necesite la intervención conjunta de ambos para el control clínico del dolor, por vía telefónica o presencial.
Conclusiones
El dolor neuropático es el causado por una lesión o enfermedad del sistema nervioso somatosensorial. Representa un problema sociosanitario de gran envergadura, que afecta a un grupo importante de población (5-8 %). Es el resultado de múltiples causas y puede presentarse como una gran variedad de síndromes.
El diagnóstico es clínico: la anamnesis y la exploración son fundamentales. Los descriptores clínicos y la exploración del sistema somatosensorial son las claves.
El tratamiento es multimodal y pueden proponerse medidas no farmacológicas y farmacológicas. La mayor parte de las guías de práctica clínica consultadas coinciden en señalar que los antidepresivos tricíclicos (particularmente amitriptilina), los duales (particularmente duloxetina) y los antiepilépticos gabapentina/pregabalina, constituyen los fármacos de primera línea en el tratamiento del dolor neuropático; el tramadol, los apósitos de lidocaína al 5 % y parches de capsaicina al 8 % son fármacos de segunda línea; los opioides potentes constituyen una tercera línea de tratamiento.
Es necesario un mejor conocimiento y entendimiento mutuo de los médicos de atención primaria y las UTD, que garantice una adecuada coordinación y continuidad de los cuidados en pacientes con dolor neuropático.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Tick H, Nielsen A, Pelletier KR, Bonakdar R, Simmons S, Glick R et al. Evidence-Based Non pharmacologic Strategies for Comprehensive Pain Care. Explore (NY). 2018; 14: 177-211.
- Majeed MH, Sudak DM. Cognitive behavioral therapy for chronic pain — one therapeutic approach for the opioid epidemic. J Psychiatr Pract. 2017; 23: 409-14.
- Geneen LJ, Moore RA, Clarke C, Martin D, Colvin LA, Smith BH. Physical activity and exercise for chronic pain in adults: an overview of Cochrane Reviews. Cochrane Database Syst Rev. 2017; 1: CD011279.
- Ju ZY, Wang K, Cui HS, Yao Y, Liu SM, Zhou J, et al. Acupuncture for neuropathic pain in adults. Cochrane Database Syst Rev. 2017; 12: CD012057.
- Gibson W, Wand BM, O’Connell NE. Transcutaneous electrical nerve stimulation (TENS) for neuropathic pain in adults. Cochrane Database Syst Rev. 2017; 9: CD011976.
- González-Escalada JR, Rodríguez MJ, Camba MA, Portolés A, López R. Recomendaciones para el tratamiento del dolor neuropático. Rev Soc Esp Dolor. 2009; 16: 445-67.
- Martínez-Salio A, Gómez A, Ribera MV, Montero J, Blanco E, Collado A, et al. Diagnóstico y tratamiento del dolor neuropático. Med Clin (Barc). 2009; 133: 629-36.
- Attal N, Cruccu G, Baron R, Haanpää M, Hansson P, Jensen TS, et al. EFNS guidelines on he pharmacological treatment of neuropathic pain: 2010 revision. Eur J Neurol. 2010; 17: 1113-e88.
- Neuropathic pain in adults: pharmacological management in non-specialist settings. NICE Guidelines (Last updated April 2018) [Internet] [consultado 9 enero 2020]. Disponible en: https://www.nice.org.uk/guidance/cg173/resources/neuropathic-pain-in-adults-pharmacological-management-in-nonspecialist-settings-pdf-35109750554053
- Mu A, Weinberg E, Moulin DE, Clarke H. Pharmacologic management of chronic neuropathic pain: Review of the Canadian Pain Society consensus statement. Can Fam Physician. 2017; 63: 844-52.
- Finnerup NB, Attal N, Haroutounian S, McNicol E, Baron R, Dworkin RH, et al. Pharmacotherapy for neuropathic pain in adults: a systematic review and meta-analysis. Lancet Neurol. 2015; 14: 162-73.
- Alcántara Montero A, Sánchez Carnerero CI. Actualización en el manejo de la neuralgia del trigémino. Semergen. 2016;42:244-53.
- Alcántara Montero A, Ibor Vidal PJ, Alonso Verdugo A, Trillo Calvo E. Actualización en el tratamiento farmacológico del dolor neuropático. Semergen. 2019; 45: 535-45.
- Alcántara Montero A, Sánchez Carnerero CI, Goicoechea García C. Terapias emergentes en desarrollo clínico y nuevas aportaciones en dolor neuropático. Rev Esp Anestesiol Reanim. 2019; 66: 324-34.
- Gálvez R, Blanco E, Ibor PJ, Pérez C, Serrano A. Protocolo de derivación de Atención Primaria a Unidades del Dolor para pacientes con Dolor Neuropático. Avalado por SED y SEMERGEN. 2017.