Original
Información del artículo
Historia del artículo:
Recibido el 14 de julio de 2021
Aceptado el 14 de noviembre de 2022
On-line el 13 de enero de 2023
Palabras clave:
Cáncer de testículo
Masa escrotal
*Autor para correspondencia
Correo electrónico:
mefren.urologia@gmail.com
(M.E. Jiménez Romero)
Keywords:
Testicular cancer
Scrotal mass
Isabel Bueno Gonzáleza, Ana Santaella Garcíab, Miguel Efrén Jiménez Romeroa,*
aServicio de Urología, Instituto de Investigación e Innovación Biomédica de Cádiz (INiBICA). Área de Gestión Sanitaria Campo de Gibraltar Este. Hospital de la Línea de la Concepción. Universidad de Cádiz, Cádiz. bServicio de Medicina Familiar y Comunitaria. Centro de Salud Ribera del Muelle (Puerto Real). Distrito Bahía de Cádiz-La Janda. Cádiz.
Resumen
El cáncer de testículo representa el 1 % de las neoplasias en varones y el 5 % de todos los tumores urológicos. Es más frecuente entre los 15 y 35 años de edad. Solo el 1-2 % de los casos se presenta de forma bilateral en el momento del diagnóstico1.
Dejado a su evolución natural, conduce a la muerte al 85 % de los afectados en el curso de 2 a 5 años. Sin embargo, gracias a la mejora de los métodos diagnósticos y a un tratamiento más eficaz, es uno de los tumores malignos con menor mortalidad.
Proponemos directrices con el objetivo de agilizar y facilitar el papel del médico de atención primaria ante el diagnóstico de una masa escrotal. Exponemos claves epidemiológicas, clínicas y analíticas que sirvan a estos profesionales para prever el diagnóstico más probable e identificar las pruebas diagnósticas necesarias a solicitar desde sus consultas.
© 2022 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Testicular cancer: diagnostic keys in primary care and review of clinical guidelines
Abstract
Testicular cancer represents 1% of malignancies in males and 5% of all urological tumors. It is more frequent between ages 15 to 35 years. Only 1-2% of the cases occur bilaterally at the time of the diagnosis.1
Left to its natural evolution, it leads to the death of 85% of those affected within the course of 2 to 5 years. However, thanks to the improvement of the diagnostic methods and to a more effective treatment, it is one of the malignant tumors with less mortality.
We propose guidelines with the aim of accelerating and facilitating the role of the primary care physician in the diagnosis of a scrotal mass. We describe epidemiological, clinical and analytical keys that serve these professionals to anticipate the most likely diagnosis and to identify the necessary diagnostic tests to request from their consultations.
© 2022 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Varón de 32 años de edad, que acude a la consulta de Atención Primaria tras la palpación de una pequeña tumoración en el testículo derecho hace algo más de una semana. Niega traumatismo testicular previo, ni haber mantenido relaciones sexuales de riesgo, ni clínica miccional asociada a este hallazgo, ni aumento del volumen escrotal ni dolor testicular.
Durante la exploración, su médico de cabecera aprecia una masa intratesticular derecha, indolora, de consistencia dura, de unos 2 cm aproximadamente.
Ante estos hallazgos, decide remitirlo a consulta de Urología por vía urgente para valoración de la lesión testicular.
Allí se descubre una masa pétrea, fija e indolora en el polo superior del teste derecho.
La ecografía testicular revela una masa heterogénea de características malignas.
Los marcadores tumorales se encuentran dentro de los límites de la normalidad.
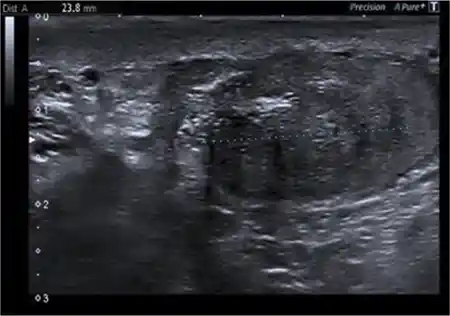
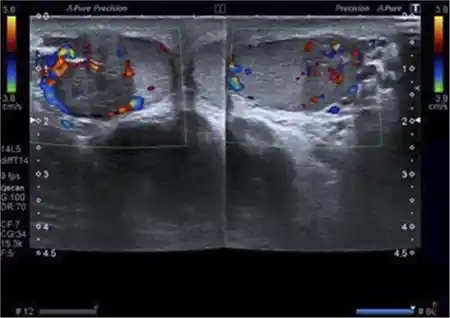
En la ecografía-doppler testicular se visualiza una lesión sólida heterogénea, de 16 x 15 mm en el interior del testículo derecho, con aumento de su vascularización (figura 1). A su vez, en el testículo izquierdo se aprecia una lesión de características similares, aunque menos definida y de menor tamaño (10 mm de diámetro), también con aumento de su vascularización (figura 2).
No se encontraron signos de enfermedad metastásica a distancia tras la valoración con TAC torácica y abdómino-pélvica.
Con estos hallazgos, y ante la presencia de dos lesiones testiculares sincrónicas, de características semejantes, se presenta en Sesión Clínica del Servicio de Urología y en el Comité de Tumores Urológicos Multidisciplinar. Se determina realizar orquiectomía radical derecha por vía inguinal en primer lugar, para posteriormente, y en función del resultado anatomopatológico, considerar la orquiectomía radical izquierda. Antes de la intervención, se determina criopreservación de semen (por la alta probabilidad de anorquia y de tratamiento quimioterápico adyuvante).
El resultado histopatológico del testículo derecho confirmó la presencia de un tumor de células de Leydig, sin componentes neoplásicos malignos. Una exhaustiva revisión bibliográfica sobre este tipo de tumores desvela un bajo, aunque no despreciable, porcentaje de malignidad asociado a estos, con rápida transformación en tumores agresivos y alta tasa de metástasis tempranas (10 % de los casos).
A pesar de ello, se decide vigilancia activa de la lesión testicular izquierda con revisiones trimestrales.
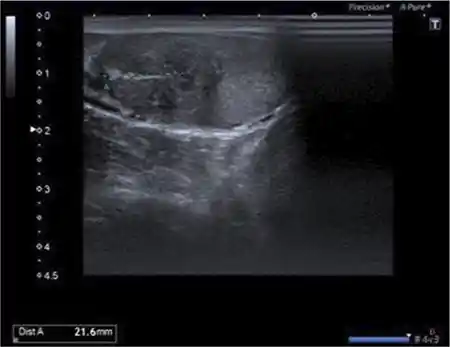
En la primera revisión, una nueva ecografía-doppler testicular desvela que la lesión sólida izquierda presenta un diámetro de 21 mm, lo que significa haber doblado su tamaño con respecto al estudio previo (figura 3).
Tras consenso en el Comité de Tumores y diálogo con el paciente, se propone y decide orquiectomía radical izquierda por vía inguinal tras nueva preservación de semen.
La anatomía patológica de la pieza informa nuevamente de la existencia de un tumor benigno de células de Leydig.
Tras ello, se remite a consulta de Endocrinología para inicio de terapia hormonal sustitutiva. Permanece en tratamiento con inyecciones trimestrales de testosterona.
Se establece seguimiento en consulta de Uro-Oncología, con solicitud de marcadores tumorales y TAC torácica y abdómino-pélvica semestrales.
En este caso en concreto, la gestión de Atención Primaria resultó clave tras la derivación urgente a la consulta de Urología, lo que llevó a un rápido diagnóstico y tratamiento.
Figura 1 – Lesión sólida heterogénea intratesticular derecha.
Figura 2 – Aumento de vascularización en ambas lesiones testiculares.
Figura 3 – Aumento de tamaño de la lesión sólida intratesticular izquierda en ecografía de control.
Comentario
Toda masa escrotal dura e indolora debe orientarse como tumoral mientras no se demuestre lo contrario. Tras una minuciosa exploración física, la ecografía testicular y la determinación sérica de marcadores testiculares (B-HCG y AFP) pueden ser suficientes para confirmar la presencia de un tumor testicular en un 90 % de los casos. La presencia de marcadores elevados asegura la malignidad de la masa, pero su negatividad no descarta malignidad, lo que obliga a una exploración intraoperatoria del testículo.
Entre los factores de riesgo para el desarrollo de cáncer testicular se han descrito antecedentes de criptorquidia o testes no descendidos (síndrome de disgenesia testicular), síndrome de Klinefelter, antecedentes familiares de primer grado (padre/hermano), tumor o neoplasia intratubular contralateral e infertilidad1.
La forma más frecuente de presentación es como un nódulo indoloro unilateral de reciente aparición. Sin embargo, hasta un 20 % de los pacientes pueden presentar dolor escrotal intenso en el momento del diagnóstico. Otras formas de presentación menos frecuentes son dolor lumbar, en el flanco y ginecomastia. Resulta importante mencionar que hasta un 10% pueden imitar clínicamente a una orquiepididimitis1, lo cual retrasa el diagnóstico correcto. En casos avanzados pueden presentar síntomas sistémicos, tales como pérdida de peso o astenia2.
Ante la presencia de una masa testicular, el método de excelencia para el diagnóstico inicial consiste en una exploración física minuciosa, ecografía testicular, solicitud de marcadores tumorales testiculares y petición de seminograma.
Sospecha diagnóstica en atención primaria
La anamnesis y la exploración física constituyen el eje principal en el diagnóstico inicial. A su vez, las pruebas complementarias (analítica con marcadores tumorales y ecografía testicular) ayudarán a orientar el estudio y descartar la presencia de patología que requiera tratamiento urgente3.
La anamnesis debe centrarse en la evaluación de los siguientes antecedentes: infección urinaria, ausencia de testículo, tratamiento de la ectopia, cirugía inguinal de la hernia y edad de la pubertad.
Es importante conocer las características del dolor, ya que si este se presenta será un síntoma clave para la orientación diagnóstica inicial4. Debemos interrogar sobre el inicio, duración, intensidad e irradiación del mismo.
También habrá que centrarse en los siguientes signos asociados: aumento de volumen escrotal, disuria, polaquiuria, exudado uretral, hemospermia, fiebre y alteración del estado general5.
Durante la exploración física hay que llevar a cabo una valoración de los distintos constituyentes de la bolsa escrotal: del propio escroto, del testículo, del epidídimo y del cordón.
La exploración del escroto permite apreciar los pliegues, la pilosidad y el grosor de las capas, y evaluar si existe alguna anomalía. El reflejo cremastérico desaparece durante una torsión del cordón espermático. También hay que descartar la presencia de hidrocele.
El testículo es un órgano par, ovoide, que en condiciones normales se sitúa en la parte baja de la bolsa escrotal. Sus dimensiones medias son de 4-5 cm de longitud. Se han de palpar ambos testes con suavidad, cogiéndolos entre el pulgar y los dedos índice y medio para poder evaluar correctamente su tamaño, forma, consistencia, movilidad y posición. Toda masa dura, indolora o fija debe considerarse tumoral hasta que se demuestre lo contrario. Con la palpación se debe apreciar:
- Posición: si es alta, puede deberse a una anomalía de la migración (testículo en ascensor o ectópico), o a una torsión del cordón espermático (si se asocia a dolor intenso).
- Sensibilidad: un dolor agudo muy intenso, que dificulta la exploración, orienta a torsión del cordón espermático; un dolor menos agudo y asociado a inflamación testicular puede orientarnos hacia orquitis u orquiepididimitis.
- Forma y consistencia: en presencia de tumor, podemos encontrar un testículo aumentado de tamaño, indurado e irregular.
- Volumen: la evaluación del volumen es un criterio para apreciar la función testicular.
El epidídimo tiene una longitud de unos 5 cm y rodea la parte posterosuperior del testículo. Patológicamente se puede producir una inflamación de origen infeccioso, dolor con la palpación, fiebre o clínica miccional.
El cordón espermático se sitúa entre el testículo y el trayecto inguinal y está compuesto por el conducto deferente y varias estructuras vasculares. Patológicamente las venas pueden estar dilatadas, en cuyo caso son palpables y constituyen el varicocele. La exploración de estas venas dilatadas se ve favorecida por la bipedestación y la maniobra de Valsalva6.
Las pruebas complementarias que pueden ayudar a orientar y acelerar el proceso diagnóstico son las siguientes:
- Hemograma/bioquímica de sangre y sistemático de orina: especialmente útiles ante la sospecha de procesos infecciosos/inflamatorios3.
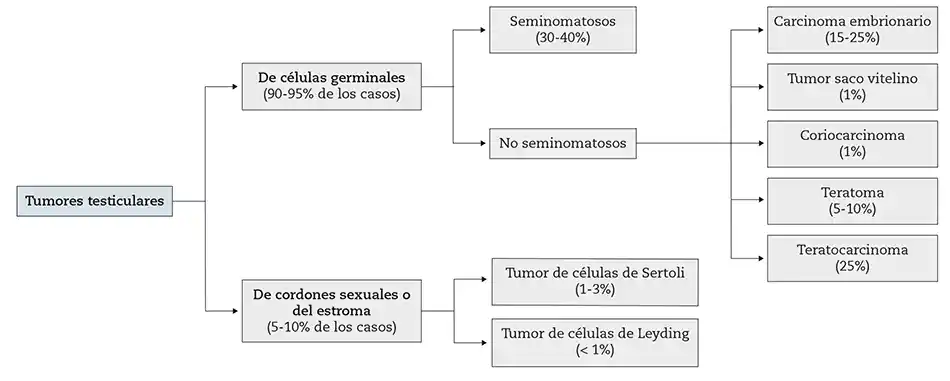
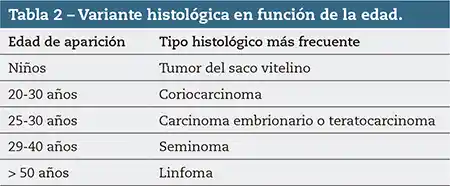
- Marcadores tumorales del testículo: son valiosos tanto para el diagnóstico (antes de la orquiectomía) como para el pronóstico (después de la orquiectomía se negativizan)1. No se debe olvidar, sin embargo, que su negatividad no excluye el diagnóstico3. En la figura 4 ofrecemos información práctica sobre la variante histológica de los tumores testiculares y su frecuencia1. En las tablas 1 y 2 se muestra la relación de los marcadores y de la edad del paciente en el momento del diagnóstico con la probable naturaleza histológica del tumor.
- Pruebas de imagen: la ecografía-doppler testicular es la prueba más sensible, ya que aporta información sobre la masa y la relación de esta con el resto de las estructuras testiculares5; debe ser solicitada ante cualquier sospecha clínica de tumor testicular y en varones jóvenes con masas retroperitoneales o viscerales o B-HCG o AFP séricas elevadas, o que consulten por problemas de fertilidad y sin una masa testicular palpable1. Algunos centros de salud disponen de ecógrafos y muchos médicos de atención primaria ya están formados o en proceso de aprendizaje.
Síndrome escrotal agudo en atención primaria: diagnóstico diferencial
Debe hacerse fundamentalmente con la torsión testicular evolucionada, la torsión de apéndices testiculares y con los procesos inflamatorios como la epididimitis y la orquiepididimitis.
En el algoritmo de la figura 5 se exponen los datos para una correcta aproximación diagnóstica.
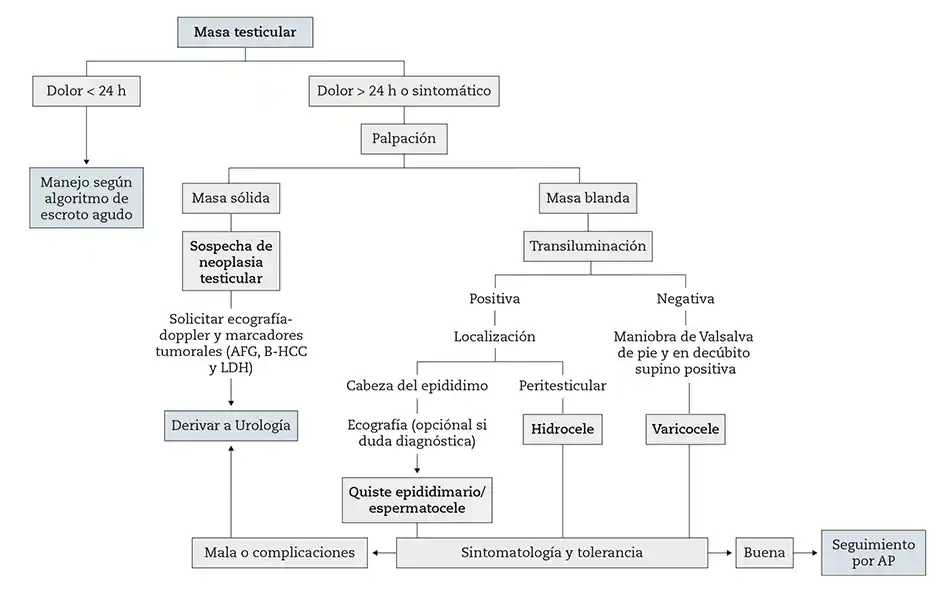
En el algoritmo de la figura 6 se expone el abordaje de una masa testicular en atención primaria.
Figura 4 – Clasificación histológica de tumores de testículo y frecuencia.
Figura 5 – Diagnóstico diferencial escroto agudo.
Figura 5 – Abordaje de una masa testicular.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Albers P, Albrecht W, Algaba F, Bokemeyer C, Cohn-Cedermark G, Fizazi K, et al. EAU Guidelines on testicular cancer. European Association of Urology; 2019.
- Broseta E, Budía A, Burgués JP, Luján S. Tumores germinales de testículo. Urología Práctica. 4ª ed. Barcelona: Elsevier; 2016. p. 371-82.
- Pérez D, Morera M. Mejorando la capacidad resolutiva. Masa escrotal. AMF. 2014; 10(8): 450-4.
- Monge Ropero, N., Calvo Cebrián, A., Gómez Moreno, R., Cebrián Patiño, E. Valoración del síndrome escrotal agudo en Atención Primaria. Med Integral. 2003; 41(1): 4-7.
- Guy L, Védrine N. Exploración clínica y de laboratorio del testículo. EMC. Elsevier Masson; 2008
- Wein A, Kavoussi L, Novick A, Partin A, Peter C. Campbell-Walsh: Urología. 10ª ed. México, D.F: Editorial Médica Panamericana; 2015.