Artículo Original
Información del artículo
Historia del artículo:
Recibido el 21 de enero de 2021
Aceptado el 30 de marzo de 2021
On-line el 21 de julio de 2021
Palabras clave:
Fibrilación auricular
Anticoagulantes
Trombosis
Seguridad del paciente
*Autor para correspondencia
Correo electrónico:
fatienzam@hotmail.com
(F. Atienza).
Keywords:
Atrial fibrillation
Anticoagulants
Thrombosis
Patient safety
Francisco Atienzaa,*, María Isabel Egocheagab, Rafael Hidalgoc, Núria Marínd, Annalisa Péreze, Vivencio Barriosf
aUnidad de Gestión Clínica Virgen de África. Sevilla. bCentro de Salud Isla de Oza. Madrid. cUnidad de Gestión de Cardiología y Cirugía Cardiovascular. Hospital Universitario Virgen de Macarena. Sevilla. dBayer. Barcelona. eGOC Networking. Barcelona. fDepartamento de Cardiología. Hospital Universitario Ramón y Cajal. Madrid.
Resumen
Objetivos. El propósito de este trabajo es dar seguimiento al proyecto realizado en 2017, donde se contribuía a la mejora del proceso de la anticoagulación en pacientes con fibrilación auricular no valvular (FANV) y riesgo elevado de ictus, mediante acciones de sensibilización y formación al colectivo de médicos especialistas en medicina familiar y comunitaria. En este trabajo se han priorizado las recomendaciones sugeridas en los talleres AMFE (Análisis Modal de Fallos y Efectos) realizados durante 2017. Se identificaron factores clave de éxito y barreras para las recomendaciones más prioritarias, se realizó un plan operativo para la implementación de dichas recomendaciones y se identificaron todas las acciones necesarias para poder llevarlo a cabo, así como propuestas de distribución de responsabilidades, si procedía.
Materiales y métodos. Se realizaron 30 talleres con la contribución de 59 ponentes (especialistas en cardiología y medicina familiar) y la participación de 323 médicos de familia de ámbito nacional. El trabajo de campo se extendió entre el 22 de febrero y el 26 de junio de 2018.
Resultados. Las recomendaciones priorizadas por los participantes fueron: (a) valorar el cambio de tratamiento a ACOD; (b) realizar un seguimiento adecuado a los pacientes; y (c) realizar protocolos o guías de práctica clínica sobre FANV. Para cada una de ellas se determinaron los factores de éxito y las barreras para llevarlas a cabo. Finalmente, se definió el plan operativo de cada uno de ellos. Los asistentes concluyeron que un factor clave de éxito en las recomendaciones fue valorar el cambio de tratamiento a ACOD y que para realizar un seguimiento adecuado al paciente sería clave la formación a los médicos de familia; esta debería correr a cargo de un equipo multidisciplinar con el apoyo de la Industria Farmacéutica y de las Sociedades Científicas.
Conclusiones. Los asistentes a los talleres consideraron que para la mejora del proceso de la anticoagulación en pacientes con FANV es necesario valorar el cambio de tratamiento a ACOD, realizar un seguimiento adecuado a los pacientes o realizar protocolos o guías de práctica clínica sobre FANV. Para ello dibujaron planes operativos y destacaron la necesidad de formación a los médicos de familia.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Proposals to improve the management of patients anticoagulated with non-valvular atrial fibrillation and risk of stroke
Abstract
Objectives. The purpose of this work is to provide a follow-up to the project carried out in 2017, in which the sensitization actions and training given to the group of medical specialists in family and community medicine contributed to the improvement of the anticoagulation process in patients with non-valvular atrial fibrillation (NVAF) and elevated risk of stroke. In this work, priority has been given to the recommendations suggested in the FMEA (Failure Mode and Effects Analysis) workshops conducted during 2017. Key factors of success and barriers for the recommendations with the greatest priority were identified. An operation plan for the implementation of said recommendations was made. In addition, all the actions necessary to be able to carry it out as well as proposals for distribution of responsibilities, if pertinent, were made.
Material and methods. A total of 30 workshops with the contribution of 59 speakers (specialists in cardiology and family medicine) and the participation of 323 family physicians on a national level were carried out. The field work was conducted between 22 February and 26 June of 2018.
Results. The recommendations given priority by the participants were: (a) to evaluate the change of treatment to DOAC; (b) to conduct an adequate follow-up to the patients; and (c) to carry out protocols or clinical practice guidelines on NVAF. The factors of success and barriers to carry them out were determined for each one of them. Finally, an operation plan was defined for each one of them. The participants concluded that a key success factor in the recommendations was to evaluate the change of treatment to DOAC and that the training to the family physicians would be a key factor to an adequate follow-up of the patients. This should be the responsibility of a multidisciplinary team with the support of the Pharmaceutical Industry and the Scientific Societies.
Conclusions. The participants in the workshops considered that in order to improve the anticoagulation process in patients with NVAF, it is necessary to evaluate the change of treatment to DOAC, to conduct an adequate follow-up to the patients or to made protocols or clinical practice guidelines on NVAF. To do so, they made operation plans and stressed the need for training of the family physicians.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Introducción y objetivos
Tal como muestran diversos estudios independientes, la fibrilación auricular (FA) es la arritmia más común1-8, tanto en España como más allá de nuestras fronteras9-11. Suele asociarse a hipertrofia ventricular izquierda11, 12, insuficiencia cardiaca, deterioro cognitivo e ictus.
La guía de la Sociedad Europea de Cardiología, publicada en agosto de 201613, y el consenso NICE14 consideran que los anticoagulantes orales directos (ACOD) tienen un perfil beneficio-riesgo favorable. Estos han demostrado reducir significativamente los ictus y las hemorragias intracraneales, así como de la mortalidad por cualquier causa, si bien producen un aumento del riesgo de sangrado gastrointestinal. Además, varios estudios observacionales recientes realizados en España15-19 muestran que casi la mitad de los pacientes con fibrilación auricular no valvular (FANV) anticoagulados con antagonistas de la vitamina K (AVK) en el ámbito de la atención primaria (AP) presentaban un control de la anticoagulación inadecuado.
Así pues, con el fin de mejorar la anticoagulación en pacientes diagnosticados de FANV, se realizaron varios talleres adaptados del método de Análisis Modal de Fallos y Efectos (AMFE) 20. El objetivo de dichos talleres fue realizar acciones de sensibilización al colectivo de médicos de familia por medio de un proceso de participación estructurado cuyos objetivos operativos fueron:
- Identificar los fallos y las causas que motivan un episodio trombótico o hemorrágico en pacientes con FANV.
- Planificar acciones de mejora para prevenir la aparición de los fallos y mejorar su posible detección.
- Disminuir las incertidumbres que pueden existir en el abordaje de los pacientes con FANV anticoagulados.
Entre las conclusiones de este proyecto se destaca que existe una percepción generalizada entre los médicos de familia de que «el abordaje de la FANV constituye un importante problema asistencial y que existe un amplio sector de estos pacientes sin cobertura terapéutica de anticoagulación efectiva (no anticoagulados o anticoagulados deficientemente), lo que incrementa su riesgo de ictus, así como también de presentar hemorragias de mayor o menor gravedad».
Mayoritariamente, los participantes en este proyecto consideraron que para paliar este problema era necesario:
- Realizar un seguimiento adecuado de los pacientes con FANV.
- Realizar o actualizar protocolos y guías de práctica clínica sobre el diagnóstico, abordaje y tratamiento de la FANV.
- Realizar formación continuada a las diferentes especialidades implicadas en la FANV (medicina de familia, enfermería, cardiología, hematología, neurología…) de forma conjunta en los centros de salud sobre el diagnóstico, abordaje y tratamiento de la FANV; y en concreto, sobre los ACOD para promover su uso.
Por consiguiente, el propósito de este nuevo proyecto ha sido:
- Priorizar las recomendaciones sugeridas en los talleres AMFE en 2017.
- Identificar factores clave de éxito y barreras para las recomendaciones más prioritarias.
- Realizar un Plan Operativo para la implementación de dichas recomendaciones e identificar todas las acciones necesarias para poder llevarlo a cabo, así como posibles responsables, si procede.
Métodos
Entre el 22 de febrero y el 26 de junio de 2018 se realizaron 30 talleres que contaron con la contribución de 59 ponentes (especialistas en cardiología y en medicina de familia) y la participación 323 médicos de AP procedentes de 9 comunidades autónomas. En el proyecto que precedía al presente trabajo, entre marzo y junio de 2017, se realizaron 38 talleres de grupos focales en los que participaron 482 médicos (444 de AP y 38 cardiólogos) de ámbito nacional con representación geográfica homogénea20.
Al inicio de cada taller, un médico de familia impartía una ponencia que tenía por objetivo explicar el reto que supone entre la comunidad científica la prevención del ictus en pacientes con FA. Posteriormente, este procedía a la presentación de infografías con los resultados de los fallos y causas priorizados en los talleres AMFE realizados en 2017 (Fig. 1A y 1B).
A continuación, los participantes, divididos aleatoriamente en dos grupos, priorizaban las recomendaciones extraídas de los talleres AMFE 2017 de mayor interés. Para ello, primero el ponente explicaba las diferentes recomendaciones. A continuación, cada asistente debía priorizar dos sobre las que le gustaría centrar el plan de acción. Para ello, disponían de 2 pegatinas, se levantaban y las pegaban en el panel que contenía la infografía. A continuación, el moderador de la reunión, mostraba la recomendación de episodio trombótico y episodio hemorrágico con mayor número de votos.
Cada uno de los grupos trabajaba un episodio; luego, un portavoz de cada grupo presentaba y compartía en plenaria las conclusiones.
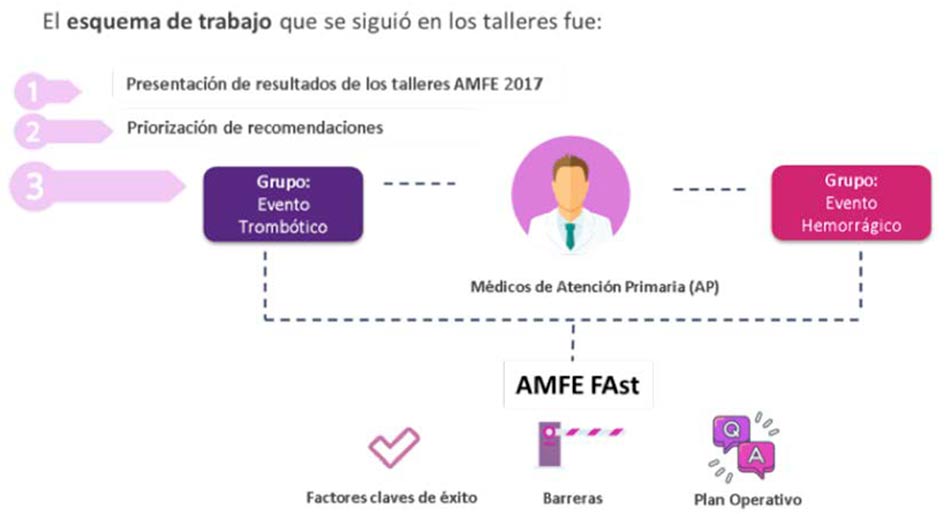
La dinámica de trabajo de cada grupo era la siguiente (Fig. 2):
- Identificación de los factores claves de éxito para implementar dicha recomendación.
- Identificación de las barreras que será necesario superar.
- Plan Operativo.
El plan operativo consistía en identificar:
- Qué acciones se deberían llevar a cabo para realizar un protocolo; en el caso de que ya existiera algún protocolo, que acciones se deberían llevar a cabo para implementarlo.
- Quién debería hacer estas acciones.
- Dónde se deberían hacer.
- Cómo se deberían hacer.
- En la medida de lo posible, también se establecieron indicadores en los puntos que se considerara.
Al finalizar el plan operativo, el cardiólogo, que había participado como consultor durante el taller, realizaba una ponencia con la finalidad de atender a dudas, preguntas o cuestiones que los médicos de familia podían plantear después de su activa participación en el taller. Por último, ambos ponentes cerraban la reunión con las conclusiones y aprendizajes de la misma.
Material y resultados
Evolución de la primera ola
A partir de los informes generales del Instituto de Salud Carlos III (ISCIII) del Ministerio de Sanidad (MS), el documento del 28 de febrero confirma 31 sintomáticos de covid-19, distribuidos en Andalucía (6), Baleares (1), Canarias (6), Castilla y León (2), Cataluña (3), Comunidad Valenciana (8) y Madrid (5)5. El 58 % de la muestra (18 casos) fueron notificados a través del Sistema de Vigilancia en España (SiVies) del Centro Nacional de Epidemiología: 14 eran hombres y 4 mujeres; edad media 41 años; fiebre (88 %), tos (57 %) y escalofríos (50 %) como los síntomas más frecuentes. De ellos 15 procedían del exterior (83 %) y los 3 restantes (17 %) eran resultado de transmisión comunitaria. En posteriores actualizaciones del ISCIII (2020b), los primeros contagios aparecieron el 31 de enero, y no el 28 de febrero como lo indican los Informes Generales (ISCIII, 2020a). Por su mayor veracidad, la evidencia del trabajo se basa exclusivamente en las series de tiempo de esta primera fuente.
Sin tomar en cuenta –momentáneamente– la densidad poblacional de cada comunidad autónoma, Madrid y Cataluña consolidaron desde el inicio de la emergencia (31 de enero)6 los dos focos de infección más importantes de España: aproximadamente el 50 % del total de contagios (Fig. 1). En el lado opuesto del recuento, Ceuta y Melilla contribuyen históricamente con menos del 1 % nacional. De las 15 comunidades restantes, Andalucía, Castilla y León, Castilla-La Mancha, Comunidad Valenciana y País Vasco componían la parte alta de la media (alrededor del 30 %); la parte baja, Aragón, Asturias, Baleares, Canarias, Cantabria, Extremadura, Galicia, Región de Murcia, Navarra y La Rioja (menos del 20 %). La distribución de decesos siguió la misma inercia.
Con la implementación del primer “Estado de Alarma” del gobierno central (provisionalmente del 15 al 29 de marzo)7, se restringió la circulación nacional a salidas concretas como la adquisición de alimentos y medicamentos, asistencia sanitaria o acudir al trabajo y causas de fuerza mayor (las fronteras internas se cerraron una semana después). Hasta este punto (15 de marzo), todo el territorio acumuló (información publicada el 20 de junio) 11.488 positivos: 41 % estaban hospitalizados, 8 % en cuidados intensivos y 3 % fallecidos. Corea del Sur con una población, media de edad y esperanza de vida similares a España empezó a actuar el 20 de febrero, cuando apenas registraba un centenar de enfermos8.
Durante la primera prórroga del confinamiento domiciliario (del 30 de marzo al 12 de abril), el país ascendió al tercer y segundo lugar mundial en diagnósticos confirmados y pérdidas mortales, respectivamente. Siguiendo el informe n° 71 de la OMS, el 31 de marzo existían 750.890 casos, con Estados Unidos como nuevo epicentro de la pandemia (140.640), Italia (101.739) y España (85.195); de las 36.405 defunciones, Italia sumaba 32 % (11.591), España 20 % (7.340) y China 9 % (3.314)4. En posteriores actualizaciones (18 de septiembre), las ciudades de Ceuta y Melilla concentraban –al inicio de la prorroga– 220 personas contagiadas; las 17 comunidades más de mil cada una: Madrid (51.457), Cataluña (30.707), la parte alta de la media entre 9 mil y 13 mil, y la parte baja entre mil y 6 mil. Las diferencias entre ambos cortes de información dan cuenta del subregistro que existía –y probablemente sigue existiendo– en las cifras oficiales.
Tomando como referencia la tasa R0, que vaticana el promedio de casos secundarios de una enfermedad originados por un caso primario, la propagación del nuevo coronavirus empezó a situarse por debajo de 1 entre marzo y abril9; mientras que en el punto álgido de esta primera ola la media nacional fue superior al 3 % (inicios de marzo), el 23 de mes el primer objetivo del confinamiento empezaba a cumplirse: R0=1,04; en otras palabras: un portador del SARS-CoV-2 lo transmitía en promedio a 1,04 individuos (Fig. 2). Esto último es importante para la gestión epidemiológica, ya que a menores valores de R0 la transmisibilidad del virus disminuye, lo que se traduce en la liberación de centros y servicios sanitarios y en un lento y escalonado retorno al “nuevo orden”.
Desescalada de la primera ola
Una vez iniciada la desescalada de la primera ola, la monitorización cuantitativa de la contingencia se volcó al número total de positivos nuevos y por comunidades y ciudades autónomas: aplanamiento longitudinal de la curva de síntomas. Con base en la información del ISCIII6, España alcanzó un máximo de 10.471 casos nuevos el 20 de marzo, y en cada comunidad autónoma entre el 13 y 23 de mes (Fig. 3). Posteriormente, el país entero presentó registros diarios cada vez más pequeños; por ejemplo, el 21 de marzo aparecieron 7.208 casos nuevos (3.263 menos que el día previo); el 12 de abril (inicio de la segunda prórroga) 2.406; el 26 de abril (tercera prórroga) 653; y así hasta llegar a menos de 500 contagios el 6 de mayo (la cuarta y quinta prórroga empezaron el 10 y el 24 de mayo, respectivamente) (Fig. 4).
Con la natural ausencia de una muestra aleatoria que corrija los problemas de autoselección en la estimación real de contagios y víctimas mortales, se calcularon sus tasas per cápita considerando la cantidad de población del censo del 2019 del Instituto Nacional de Estadística (INE)10. Aunque en valores absolutos Madrid y Cataluña concentraron el 50 % de toda la estadística, las tasas de positividad de La Rioja, Navarra y Castilla y León eran las primeras de la lista: por cada mil habitantes La Rioja tenía 12,6 verificados frente a 10,9 de Madrid (Fig. 5). Los más de cinco millones de personas de la Comunidad Valenciana (cuarta en este rubro) tenían la incidencia más baja del virus (0,8 %), inferior incluso a Ceuta y Melilla, cuyas demarcaciones son decenas de veces menos pobladas.
Hasta el 30 de abril, la Comunidad de Madrid tenía la tasa de mortalidad más alta: 12,3 por cada 10 mil habitantes. A partir de mayo, Castilla-La Mancha (novena en cantidad de población) toma su lugar: 12,4 a inicios de mes y 14,4 como promedio general (Fig. 5). En contra de lo esperado, La Rioja (cuya población es la más baja de entre las comunidades autónomas) ostentaba el tercer índice de defunciones más pronunciado (11,2), superior al 7,8 de Cataluña y muy alejado del 1,6 de Andalucía (la más poblada). A la espera de un extenso estudio de seroprevalencia del SARS-CoV-211, la fotografía más realista de la situación parece provenir de las cifras en niveles per cápita, y no precisamente del examen habitual en valores absolutos.
Figura 1A – Resultados talleres AMFE 2017 (evento trombótico).
Figura 1B – Resultados talleres AMFE 2017 (evento hemorrágico).
Figura 2 – Esquema de trabajo.
Figura 3 – Recomendaciones más priorizadas del evento hemorrágico y trombótico (en conjunto)
Resultados
Tal como se aprecia en la figura 3, las tres recomendaciones priorizadas por los médicos participantes en los talleres para mejorar la anticoagulación de los pacientes diagnosticados de FANV fueron:
- Valorar el cambio de tratamiento a ACOD.
- Realizar un seguimiento adecuado a los pacientes.
- Realizar protocolos o guías de práctica clínica sobre FANV.
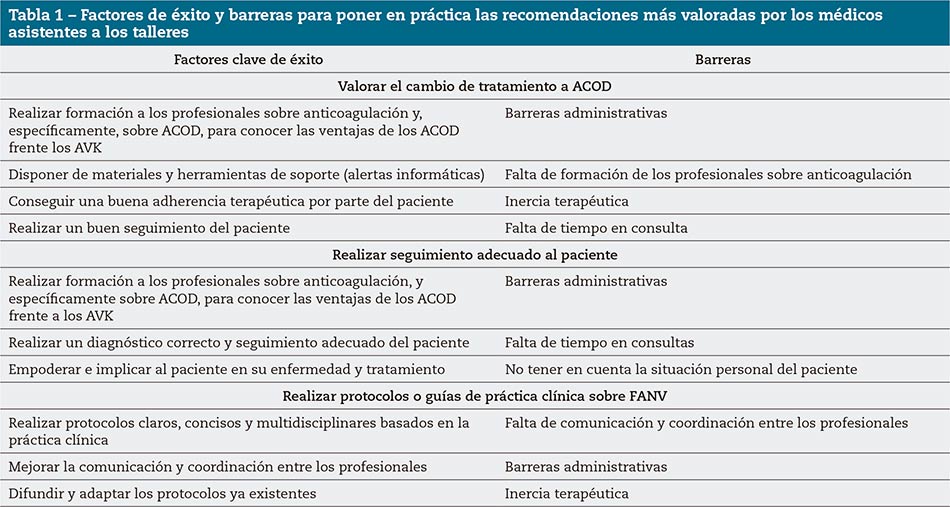
En la tabla 1 se describen los factores clave de éxito y las barreras identificadas por los médicos para las recomendaciones más valoradas (valorar el cambio de tratamiento a ACOD, realizar seguimiento adecuado al paciente y realizar protocolo o guías de práctica clínica sobre FANV).
Respecto al Plan Operativo, los médicos participantes entendieron que la formación a los médicos de familia (factor clave de éxito identificado para valorar el cambio de tratamiento a ACOD y para realizar un seguimiento adecuado al paciente) debería correr a cargo de un equipo multidisciplinar (médico de familia, hematología, cardiología y enfermería) con el apoyo de la Industria Farmacéutica y de las Sociedades Científicas; evaluarse con indicadores cuantitativos definidos previamente; y realizarse mediante talleres presenciales, interactivos y prácticos, sesiones clínicas, formaciones acreditadas y autoformación por parte del propio médico, impartidos a través de cursos on line o en los centros de trabajo habituales.
Las barreras administrativas fueron el mayor obstáculo que sería necesario superar para las tres recomendaciones priorizadas. Para ello, se considera necesario: revisar la medicación del paciente de forma presencial; programar el seguimiento según el perfil del paciente; utilizar alertas informáticas cuando el paciente se encuentre fuera de rango terapéutico; consultar los protocolos para el abordaje pre/peri operatorio; citar pacientes con INR y TRT fuera de rango y dedicar más de 10 minutos a cada uno de ellos; y evaluar las acciones realizadas mediante indicadores cuantitativos diseñados al efecto.
Finalmente, de forma mayoritaria, los participantes consideraron que el factor de éxito más determinante para cumplir con los protocolos o guías de práctica clínica sobre FANV existentes era que los protocolos fueran claros, concisos, elaborados de manera multidisciplinar y basados en la práctica clínica real. Para lograrlo, no obstante, los médicos participantes apuntaron la necesidad de superar la falta de comunicación y coordinación entre los profesionales. Las nuevas guías clínicas deberían basarse en una metodología de ruta asistencial compuesta de algoritmos y tablas, ser consensuadas por un equipo multidisciplinar de expertos (médicos de familia, enfermería, neurología, cardiología, hematología, cirugía…) y estar contenidas en una App.
Comentario
Este trabajo ha sido realizado empleando una metodología cualitativa. Incluye una técnica de dinamización de grupos focales junto con el uso de tarjetas. Fue previamente estructurada mediante la definición de una secuencia de trabajo y una adaptación ad hoc del método AMFE, cuyo uso en el ámbito de la salud es todavía escaso21-25.
Los resultados constituyen un resumen la opinión de un amplio panel de expertos procedentes de la mayoría de las comunidades autónomas (en total 30 talleres con la participación de 323 médicos procedentes de 9 CCAA). No obstante, para interpretarlos correctamente debe tenerse en cuenta que se trata de información cualitativa que muestra tendencias de opinión cualificadas, ya que corresponden a profesionales con amplia experiencia clínica.
Por ello, igual que se indicó en el proyecto que precede a este20, la presente investigación puede orientar el despliegue de otros proyectos cuyo propósito sea mejorar la atención de pacientes con riesgo elevado de episodios tromboembólicos, como el ictus, diagnosticados de FANV. Tanto en este trabajo como en el anterior20 se evidencia que el abordaje de los pacientes con FANV desde atención primaria presenta dificultades, hecho que ya se pudo observar en otros estudios15-19.
El presente proyecto ha corroborado que deben tomarse acciones como más formación del personal, un mejor seguimiento de los pacientes y protocolos multidisciplinares para abordar la anticoagulación de los pacientes con una mayor efectividad.
Las barreras administrativas, así como el poco tiempo disponible por pacientes en las consultas y la inercia terapéutica se han identificado como las mayores barreras a la hora de implementar las acciones anteriormente mencionadas.
Las limitaciones de este estudio son las propias de toda investigación cualitativa. Además, es importante tener en cuenta que la opinión predominante de los médicos participantes en este estudio no tiene por qué ser representativa de todo el colectivo de la atención primaria, si bien representa las tendencias de opinión de los expertos participantes. También cabe la posibilidad de que los médicos participantes estuvieran, en general, más motivados e interesados en la patología objeto de la investigación. Se trata, no obstante, de un sesgo que, de haberse producido, implicará que la información obtenida sea más rica y relevante.
Del conjunto de aportaciones realizadas por los participantes en estos talleres se deriva que hubo un amplio consenso en considerar que, para mejorar el grado de anticoagulación de los pacientes con FANV, es preciso actualizar y ampliar las guías clínicas y protocolos disponibles así como incrementar de forma significativa las acciones de formación sobre anticoagulación en general, y sobre uso de los ACOD en particular, dirigidas a todos los profesionales que intervienen en el tratamiento de la FANV.
Agradecimientos
Los autores manifiestan su agradecimiento a todos los participantes de las sesiones de trabajo, a la empresa GOC Health Consulting por su apoyo metodológico a lo largo de todo el proceso y a Bayer Hispania por su financiación en términos editoriales.
Apoyo financiero
Este trabajo ha contado con apoyo financiero de laboratorios Bayer.
Conflicto de intereses
Vivencio Barrios, Isabel Egocheaga, Rafael Hidalgo y Francisco Atienza declaran que no tienen conflictos de intereses en relación con esta publicación.
Nuria Marín trabaja en laboratorios Bayer.
Annalisa Pérez trabaja en GOC Networking.
Bibliografía
- Perez-Villacastin J, Perez Castellano N, Moreno Planas J. Epidemiology of atrial fibrillation in Spain in the past 20 years. Rev Esp Cardiol (Engl Ed.) 2013; 66: 561-5.
- Gomez-Doblas JJ, Muniz J, Martin JJ, Rodriguez-Roca G, Lobos JM, Awamleh P, et al. Prevalence of atrial fibrillation in Spain. OFRECE study results. Rev Esp Cardiol (Engl Ed). 2014; 67: 259-69.
- Baena-Diez JM, Grau M, Fores R, Fernandez-Berges D, Elosua R, Sorribes M, et al. Prevalence of atrial fibrillation and its associated factors in Spain: An analysis of 6 population-based studies. DARIOS Study. Rev Clin Esp. 2014; 214: 505-12.
- Barrios V, Calderón A, Escobar C, de la Figuera M, Primary Care Group in the Clinical Cardiology Section of the Spanish Society of Cardiology. Pacientes con fibrilación auricular asistidos en consultas de atención primaria. Estudio Val-FAAP. Rev Esp Cardiol. 2012; 65: 47-53.
- Zulkifly H, Lip GYH, Lane DA. Epidemiology of atrial fibrillation. Int J Clin Pract. 2018; 72: e13070.
- Gómez-Doblas JJ, López-Garrido MA, Esteve-Ruiz I, Barón-Esquivias G. Epidemiología de la fibrilación auricular. Rev Esp Cardiol. 2016; 16: 2-7.
- Dubois Marques D, Mora Llabata V, Pacheco Arroyo J, Gasull Insertis S, Vicente Cañizares M, Roldán Torres I. Adecuación del tratamiento antitrombótico en los pacientes con fibrilación auricular no valvular. Registro AFINVA. Aten Primaria. 2018; 50: 340-9.
- Polo García J, Vargas Ortega D, Formiga F, Unzueta I, Fernández de Cabo S, Chaves J. Profiling of patients with non-valvular atrial fibrillation and moderate-to-high risk of stroke not receiving oral anticoagulation in Spain. Semergen. 2019; 45: 396-405.
- Haim M, Hoshen M, Reges O, Rabi Y, Balicer R, Leibowitz M. Prospective national study of the prevalence, incidence, management and outcome of a large contemporary cohort of patients with incident non-valvular atrial fibrillation. J Am Heart Assoc. 2015; 4: e001486.
- Khan MA, Raja S, Ibrahim MS, Hammersely C. Prevalence and management of atrial fibrillation in primary care: a case study. Prim Health Care Res Dev. 2014; 15: 355-61.
- Seko Y, Kato T, Haruna T, Izumi T, Miyamoto S, Nakane E, et al. Association between atrial fibrillation, atrial enlargement, and left ventricular geometric remodeling. Scient Rep. 2018; 8: 6366.
- Proietti M, Marra AM, Tassone EJ, De Vuono S, Corrao S, Gobbi P, et al. Frequency of left ventricular hypertrophy in non-valvular atrial fibrillation. Am J Cardiol. 2015; 116: 877-82.
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. 2016; 37: 2893-62.
- NICE Guidance: Non-vitamin K antagonist oral anticoagulants (NOACs). Key therapeutic topic. Published: 26 February 2016. Disponible en: https://www.nice.org.uk/guidance/ktt16/resources/nonvitamin-k-antagonist-oral-anticoagulants-noacs-58757956094149.
- Barrios V, Escobar C, Prieto L, Osorio G, Polo J, Lobos JM, et al. Anticoagulation control in patients with nonvalvular atrial fibrillation attended at Primary Care centers in Spain: The PAULA Study. Rev Esp Cardiol (Engl Ed). 2015; 68: 769-76.
- Polo García J, Barrios Alonso V, Escobar Cervantes C, Prieto Valiente L, Lobos Bejarano JM, Vargas Ortega D, et al. Control de la anticoagulación en pacientes con fibrilación auricular no valvular en práctica clínica de atención primaria en las diferentes comunidades autónomas. Estudio PAULA. Semergen. 2017; 43: 207-15.
- Anguita Sanchez M, Bertomeu Martinez V, Cequier Fillat A, researchers Cs. Quality of vitamin K antagonist anticoagulation in Spain: Prevalence of poor control and associated factors. Rev Esp Cardiol (Engl Ed). 2015; 68: 761-8.
- Cinza-Sanjurjo S, Rey-Aldana D, Gestal-Pereira E, Calvo-Gomez C. Assessment of degree of anticoagulation control in patients with atrial fibrillation in Primary Health Care in Galicia, Spain: ANFAGAL Study. Rev Esp Cardiol (Engl Ed). 2015; 68: 753-60.
- Barrios V, Escobar C, Lobos JM, Polo J, Vargas D. Uso de los anticoagulantes orales de acción directa en atención primaria: Estudio ACTUA. Semergen. 2017; 43: 477-85.
- Atienza-Martín F, Barrios V, Egocheaga MI, Hidalgo R, Marín-Montañés N, Ramis C. El método AMFE (Análisis Modal de Fallos y Efectos) aplicado a la anticoagulación de pacientes con fibrilación auricular no valvular. Semergen. 2019; 45: 169-79.
- Alba Mesa F, Sanchez Hurtado MA, Sanchez Margallo FM, Gomez Cabeza de Vaca V, Komorowski AL. Application of failure mode and effect analysis in laparoscopic colon surgery training. World J Surg. 2015; 39: 536-42.
- Vazquez-Valencia A, Santiago-Saez A, Perea-Perez B, Labajo-Gonzalez E, Albarran-Juan ME. Utility of failure mode and effect analysis to improve safety in suctioning by orotracheal tube. J Perianesth Nurs. 2017; 32: 28-37.
- Arenas Jimenez MD, Ferre G, Alvarez-Ude F. Strategies to increase patient safety in hemodialysis: Application of the modal analysis system of errors and effects (FEMA system). Nefrologia. 2017; 37: 608-21.
- Krych AJ, Hevesi M, Desai VS, Camp CL, Stuart MJ, Saris DBF. Learning from failure in cartilage repair surgery: An analysis of the mode of failure of primary procedures in consecutive cases at a tertiary referral center. Orthop J Sports Med. 2018; 6: 2325967118773041.
- Mañes-Sevilla M, Marzal-Alfaro MB, Romero Jiménez R, Herranz-Alonso A, Sanchez Fresneda MN, Benedi Gonzalez J, et al. Análisis modal de fallos y efectos para mejorar la calidad en los ensayos clínicos. J Health Qual Res. 2018; 33: 33-47.