Clínica Cotidiana
Información del artículo
Historia del artículo:
Recibido el 23 de junio de 2020
Aceptado el 23 de agosto de 2021
On-line el 16 de noviembre de 2021
Palabras clave:
Insuficiencia renal aguda
Braquiterapia
*Autor para correspondencia
Correo electrónico:
chelo.naya.cendon@sergas.es
(C. Naya Cendón).
Keywords:
Acute renal failure
Brachytherapy
Adrián Rosende Canedo, Lorena López González, Chelo Naya Cendón*
CS O Portádego-SAP Culleredo. La Coruña.
Resumen
Se describe el caso clínico de un paciente diagnosticado de un cáncer de próstata en tratamiento con braquiterapia desde hace tres meses. Como consecuencia del mismo presenta una retención de orina y una insuficiencia renal aguda secundaria.
Este caso sucedió durante el periodo de confinamiento por la pandemia de Covid-19. Las citas solicitadas por el paciente eran telefónicas y el médico de familia, en función de cada caso, decidía y programaba la cita presencial. Teniendo en cuenta esta situación excepcional, queremos resaltar, en primer lugar, la importancia de la entrevista telefónica como filtro para decidir la atención presencial del paciente; por otra parte, el importante papel que desempeña la ecografía como herramienta de ayuda en la exploración en atención primaria, que, en el caso de este paciente, fue fundamental para establecer el diagnóstico y remitirlo sin retraso al segundo nivel asistencial.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Publicado por Ergon Creación, S.A.
Acute renal failure secondary to brachytherapy
Abstract
A clinical case is described of a patient diagnosed of prostate cancer under treatment with brachytherapy in the last three months. Due to this, the patient presents urinary retention and secondary acute renal failure.
This case occurred during the COVID-19 confinament period. Appointments requested by the patient were by telephone and the family doctor, based on each case, decided and scheduled the in-person appointment. Considering this exceptional situation, we want to stress, first of all, the importance of a telephone interview as a filter to decide on the in-person care of the patient. On the other hand, the important role of the ultrasound as a tool to help in the primary care study, which, in the case of this patient, was fundamental to establish the diagnosis and send the patient without delay to the second care level.
© 2021 Sociedad Española de Médicos Generales y de Familia.
Published by Ergon Creación, S.A.
Varón de 50 años de edad, hipertenso, diabético y con cardiopatía isquémica. Se encuentra en tratamiento con ácido acetil salicílico (150 mg), bisoprolol (5 mg), candesartán (8 mg), omeprazol (20 mg), liraglutida, metformina (850 mg), bromazepam (3 mg), lormetazepam (2 mg), escitalopram (20 mg), ezetimiba, rosuvastatina (20 mg) y tamsulosina (0,4 mg).
Fue diagnosticado de cáncer de próstata y hace tres meses se le realizó tratamiento con braquiterapia. Desde entonces presenta sensación de urgencia miccional y nicturia.
Refiere molestia de unos días de evolución en el costado derecho, que empeora con los movimientos y decúbito ipsilateral; en ocasiones se irradia al vacío derecho. No refiere cambios en la sintomatología miccional ni otra clínica por aparatos.
Durante la anamnesis en la consulta relata ligera astenia, disminución de apetito, sensación nauseosa y diarrea de unos días de evolución.
La exploración física es normal, salvo que durante la palpación abdominal llama la atención una masa en la región suprapúbica, la fosa iliaca y el vacío izquierdos, no dolorosa, de contorno liso y bien delimitada.
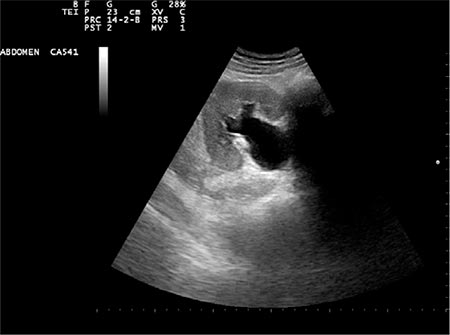
Realizamos exploración ecográfica y observamos una hidronefrosis bilateral, dilatación ureteral en su trayecto y vejiga con un volumen urinario de 1.700 cc, que se corresponde con la masa palpable.
Se realiza nueva exploración ecográfica tras la micción y se comprueba que el volumen residual es muy similar al premiccional (Figs. 1–4).
Remitimos al paciente a Urgencias del hospital para ser valorado por urología.
En la analítica de ingreso destaca una urea 256 mg/dl, creatinina 10,15 mg/dl, sodio 135 mEq/l y potasio 7,5 mEq/l.
Se le realiza sondaje vesical e inicialmente elimina 1.200 cc de orina. Queda en observación para monitorización hasta la normalización de las cifras de potasio. Posteriormente ingresa en la planta de Urología para vigilancia.
La función renal va mejorando de forma progresiva. Se procede al alta con la siguiente analítica: urea 136 mEq/l, potasio 3,58 mEq/l y filtrado glomerular 18,57. Una semana después del alta, la analítica de control muestra urea 73 mg/dl, creatinina 1,81 mg/dl y filtrado glomerular 42,35.
Figura 1 – Se observa marcada dilatación pielocalicial en el riñón derecho junto con adelgazamiento del parénquima renal.
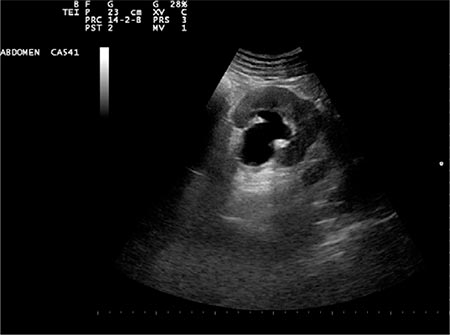
Figura 2 – Se observan los mismos hallazgos en el riñón izquierdo, lo que indica que la hidronefrosis es bilateral. Por tanto, la compresión se sitúa en el cuello vesical o en la uretra.
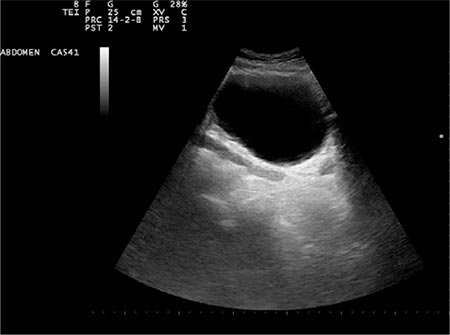
Figura 3 – Corte transversal en la zona suprapúbica, en el que se evidencia la distensión vesical junto con dilatación de ambos uréteres.
Figura 4 – Corte longitudinal: se observa la vejiga y por detrás de ella un uréter dilatado cortado por su eje mayor.
Comentario
La insuficiencia renal aguda (IRA) se define como el deterioro de la función renal en un periodo corto de tiempo, de horas a días. Este deterioro provoca la disminución del filtrado glomerular y conlleva una disminución de la capacidad para excretar los productos nitrogenados de desecho y para mantener el equilibrio hidroelectrolítico y ácido-base.
La IRA tiene un índice alto de morbimortalidad, por lo que es fundamental su diagnóstico y tratamiento precoz para prevenir la pérdida irreversible de nefronas. Las principales complicaciones que pueden poner en riesgo la vida del paciente son la hiperpotasemia, la acidosis metabólica y el exceso de volumen circulante.
La IRA se clasifica en 3 subgrupos(1):
- IRA prerrenal (55 %), causada por hipoperfusión renal: es reversible tras la corrección de la causa desencadenante.
- IRA intrínseca o parenquimatosa (40 %).
- IRA posrenal u obstructiva (5 %): originada en los uréteres, el cuello de la vejiga (la más frecuente) o la uretra.
Aunque puede ser asintomática, la IRA suele manifestarse con cambios en el volumen urinario, problemas derivados de la sobrecarga de volumen, trastornos electrolíticos y de ácido-base y signos y síntomas propios de la uremia. En la IRA prerrenal la manifestación más característica es la disminución de la diuresis; en la IRA intrínseca las manifestaciones suelen ser inespecíficas, aunque puede haber oliguria hasta en el 66 % de los casos; la IRA obstructiva es causa frecuente de anuria brusca, aunque muchos pacientes no refieren disminución de diuresis, incluso en alguna ocasión presentan poliuria e incontinencia miccional (diuresis por rebosamiento).
El diagnóstico diferencial del deterioro de la función renal se debe abordar desde cuatro puntos de vista: sindrómico (agudo o crónico), funcional (cuánto se deterioró la función renal), fisiopatológico (prerrenal, parenquimatoso o posrenal u obstructivo) y etiológico. Para ello es necesaria la realización de una correcta anamnesis y exploración física, así como la solicitud de pruebas complementarias que incluyan(2):
- Análisis de sangre: urea, nitrógeno ureico, creatinina que presente un aumento superior a 0,5 mg/dl, filtrado glomerular e iones.
- Análisis de orina: sodio urinario, osmolalidad, excreción fraccional de sodio y sedimento.
- Técnicas de imagen. La ecografía renal es el método de elección para ver la obstrucción y dilatación de la pelvis renal, aunque su sensibilidad para la obstrucción es solo del 80-85 %, ya que no siempre existe dilatación del sistema colector. En la radiografía simple de abdomen se pueden identificar cálculos radiopacos como causa de obstrucción, pero tiene limitaciones, ya que no detecta cálculos sin calcio, como los de ácido úrico.
- La biopsia renal está indicada en los casos de IRA de causa desconocida una vez descartada la patología prerrenal y posrenal.
En el tratamiento de la insuficiencia renal, e independientemente de la causa, hay que tener en cuenta:
- Medidas generales:
- Identificar y corregir factores pre y posrenales.
- Prevenir y tratar la hipoperfusión.
- Optimizar el gasto cardíaco y el flujo sanguíneo renal.
- Revisar fármacos y suspender agentes nefrotóxicos.
- Controlar el equilibrio hídrico y el peso corporal.
- Identificar y tratar las complicaciones agudas (hiperpotasemia, acidosis y edema pulmonar).
- Tratamientos específicos dirigidos a la causa:
- La causa más común de insuficiencia renal aguda es la necrosis tubular aguda. El tratamiento en este caso consiste en mantener el equilibrio electrolítico mediante la infusión de sueros y prevenir o tratar complicaciones como la infección.
- IRA prerrenal: si se recupera la normovolemia suele normalizarse la diuresis y la función renal de manera rápida.
- IRA obstructiva: es importante el diagnóstico precoz, ya que, en la mayor parte de los casos, la resolución rápida de la obstrucción permite recuperar la función del riñón obstruido.
- De forma general las indicaciones de diálisis son: hiperpotasemia grave que no responde al tratamiento médico, edema agudo de pulmón; uremia superior a 30-50 mmol/l, complicaciones graves secundarias a uremia (encefalopatía, pericarditis, neuropatía o miopatía), pH por debajo de 7,1 o sobredosis farmacológica.
La braquiterapia prostática implica la colocación de fuentes radiactivas en la glándula prostática. Debido al corto rango de radiación emitido se evita una excesiva irradiación a órganos vecinos. En los últimos años experimentó un auge muy significativo, tanto por su eficacia comparada con la cirugía como por su rapidez, reproducibilidad y escasa invasividad; sin embargo, a pesar de su carácter mínimamente invasivo y de ser una técnica generalmente bien tolerada, los pacientes tratados con braquiterapia prostática pueden presentar efectos secundarios, entre los que destacan complicaciones digestivas (fundamentalmente proctitis en un 2 % de los pacientes), disfunción eréctil (entre el 6 y el 53 % de los pacientes) y más frecuentemente complicaciones urinarias. Su máximo se alcanza entre el primer y el tercer mes posimplante, y se normaliza aproximadamente al cabo de un año. - Entre las complicaciones urinarias agudas destacan(3, 4):
- Síndrome miccional irritativo: es el efecto secundario más frecuente (46-66 % de los pacientes). Se manifiesta como escozor al orinar, frecuencia-urgencia miccional, nicturia y ocasionalmente hematuria.
- Síndrome miccional obstructivo y retención urinaria: suelen aparecer en el 50 % de los pacientes. Se manifiestan principalmente con disuria y debilidad del chorro miccional. La retención aguda de orina (RAO) ocurre habitualmente al día siguiente del implante y probablemente está relacionada con el edema post-implante y los efectos de los agentes anestésicos. Ocurre en el 5-28 % de los pacientes y se suele resolver con la colocación de una sonda vesical temporal y tratamiento con alfabloqueantes. Pocos pacientes requerirán una resección transuretral de próstata (RTUP) por retención aguda de orina (RAO) refractaria. Los pacientes con IPSS <10 tienen una incidencia de RAO del 2 %; con IPSS 10-19 del 11 %; y con IPSS>19 del 29 %.
- Como complicaciones a largo plazo se pueden encontrar:
- Estenosis uretral o del cuello vesical. Los factores para el desarrollo de este tipo de complicación son: antecedente de cirugía prostática previa al implante, la dosis que recibe la uretra bulbo-membranosa y la colocación de las semillas en posición demasiado caudal (justo anterior al ápex prostático).
- Incontinencia urinaria. Es una de las complicaciones más limitantes. Aumenta en los pacientes tratados además con radioterapia externa y sometidos a RTUP.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Naya Cendón C, Suárez Abelenda S. Guía clínica de Fisterra de Insuficiencia renal aguda. 2018. Disponible en: https://www.fisterra.com/guias-clinicas/insuficiencia-renal-aguda/
- Tenorio Cañamás MT, Rodríguez-Palomares JR, Liaño García F. Protocolo diagnóstico en el paciente con insuficiencia renal aguda. Medicine. 2015; 11: 4868-72.
- Arlaríais Guzmán S, Bonillo García MA, Broseta Rico E. Disfunción miccional post-braquiterapia en el cáncer prostático. Arch Esp Urol. 2009; 62: 826-37
- Roeloffzen EM, Hinnen KA, Battermann JJ, Monninkhof EM, van Roermund JG, van Gellekom MP, et al. The impact of acute urinary retention after iodine-125 prostate brachytherapy on health-related quality of life. Int J Radiat Oncol Biol Phys. 2010; 77: 1322-8.